Les solutions acides et basiques
I ) Rappels sur le pH d'une solution :
1) Notion de pH :
Le pH sert à mesurer le degré d'acidité d'une solution.
C'est une grandeur sans unité comprise entre 0 et 14
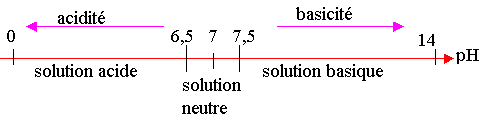
2) Mesure de pH :
On peut mesurer le pH avec du papier pH ou un pH-mètre .
L'eau a un pH neutre ( voisin de 7 )
L'acide chlorhydrique a un pH petit, inférieur à 6,5; c'est une solution acide.
La soude a un pH élevé , supérieur à 7,5 ; c'est une solution basique.
3) Dangers des solutions acides et basiques :
Ces solutions sont des produits corrosifs.
Plus ces solutions sont concentrées, plus elles sont dangereuses.
 Souvent,
pour préparer une solution, on utilise au départ une solution très concentrée
que l’on dilue avec de l’eau distillée.
Souvent,
pour préparer une solution, on utilise au départ une solution très concentrée
que l’on dilue avec de l’eau distillée.
Pour des solutions acides très concentrées,
IL NE FAUT JAMAIS VERSER L’EAU DANS L’ACIDE.
Cela peut provoquer des projections d’acide qui peuvent brûler la peau très gravement. PAS D’EAU DANS L’ACIDE
Pour diluer une solution acide concentrée, on verse la solution dans de l’eau distillée.
II ) Mesures de pH
1) Avec du papier-pH :

|
Solution |
Citron |
HCl |
vinaigre |
eau |
soude |
Eau savon |
|
pH |
|
|
|
|
|
|
|
Acide/base |
acide |
acide |
acide |
neutre |
basique |
Basique |
2) Avec un pH-mètre
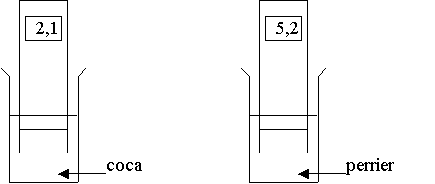
3) pH et concentration des solutions :

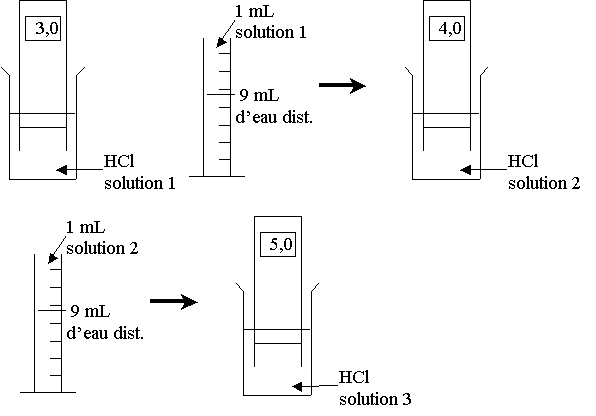
Observations : Plus l’acide chlorhydrique est dilué, plus le pH augmente.
Plus la soude est diluée, plus le pH diminue.
Interprétations : Une solution acide a un pH inférieur à 7.
Plus la solution est concentrée, plus le pH est petit.
Une solution basique a un pH supérieur à 7
Plus la solution est concentrée, plus le pH est grand.
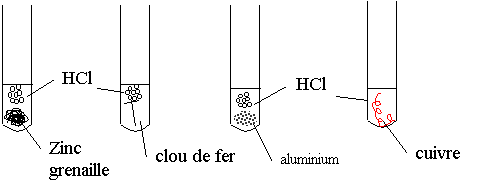
III ) Réaction avec les métaux :
1) Action de l’eau
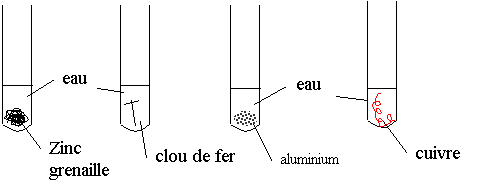
Il ne se passe rien. L'eau ne réagit pas avec les métaux.
Exemple : marmites en fonte (fer), casserole en cuivre, gouttières recouvertes de zinc…
2) Action de l'acide chlorhydrique :