1eS - Chap 05 - Conductivité molaire ionique ![]()
I ) Conductivité molaire ionique d'un ion en solution :
On appelle Λ la conductivité molaire d'une solution ionique d'un soluté unique ; elle est définie comme étant le rapport de la conductivité σ de la solution par la concentration c :
Λ = σ / c ( Λ : lambda majuscule )
 |
S.m2.mol-1 S.m-1 mol.m-3 attention unité inhabituelle
Quand la concentration c en soluté apporté est faible ( < 10-2 mol.L-1 ) , σ est proportionnelle ŕ c donc Λ ne dépend pas de c.
Λ est fonction de la nature des ions en solution.
A chaque ion d'une solution ionique, on affecte une conductivité molaire ionique désignée par la lettre λ ( en S.m2.mol-1 ).
Dans le cas d'une solution ionique d'un soluté unique contenant des ions monochargés M+aq et X-aq , on peut écrire :
Λ = λ ( M+aq ) + λ ( X-aq )
et σ = Λ . c
d'oů σ = (λ ( M+aq ) + λ ( X-aq ) ) . c
ou σ = λ ( M+aq ) . [ M+aq ] + λ ( X-aq ) . [ X-aq ]
λ se rapporte ŕ un ion donné. Elle est fonction de la température et de la nature du solvant.
λ ne dépend pas de la concentration de l'ion lorsqu'elle est faible ( ≈ 10-2 mol.L-1 )
II ) Conductivité d'une solution ionique quelconque :
Soit une solution ionique contenant p ions monochargés différents notés Xi, de concentration [Xi] et de conductivité molaire ionique λi ( i variant de 1 ŕ p ) .
La relation entre les conductivités σ de la solution s'écrit :
σ = λ1 . [X1] + λ2 . [X2] + λ3 . [X3] + ….. + λp . [Xp]
σ en S.m-1 λi en S.m2.mol-1 et [ Xi ] en mol.m-3 ATTENTION UNITE
Exemple : solution contenant des Na+, K+ , NO3- , Cl- ŕ différentes concentrations
σ = λ(Na+) . [Na+] + λ(K+) . [K+] + λ(NO3-) . [NO3-] + λ(Cl-) . [Cl-]
Remarque : La relation du paragraphe 1 est un cas particulier de cette relation.
La conductivité molaire ionique est donnée pour des concentrations faibles ( < 10-2 mol.L-1 )
III ) Conductivité molaire ionique de quelques ions monochargés :
Les mesures de conductances faites en TP sur des solutions de męme concentration comportant l'un des ions en commun, nous ont permis de constater que H3O+ et HO- ont une conductivité molaire ionique supérieure ŕ celle des autres ions.
En effet, le cas de ces ions est particulier : ils sont solvatés comme les autres ions mais forment avec les molécules d'eau une liaison assez forte appelée liaison hydrogčne.
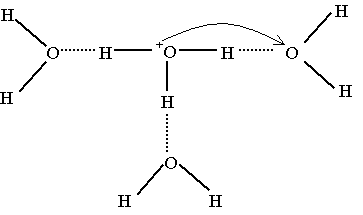
La liaison O – H est polaire.
En fait, ce n'est pas l'ion H3O+ qui se déplace, mais le proton H+ trčs petit.
Cela est plus rapide.
Pour l'ion HO- , on retrouve la męme chose, un proton H+ est fourni par une molécule d'eau voisine qui devient HO- et HO- devient H2O. Tout se passe comme si HO- se déplace alors que c'est un proton qui se déplace de proche en proche.
©Sciences Mont Blanc

