Correction - Sujet Bac ¢ Afrique - Juin 2003 ( 2,5 points)
Calculatrice autorisķe
II ) La pile Ó combustible :
1)
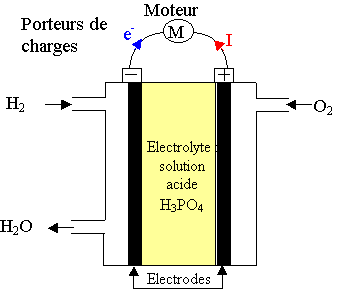 1.
Les porteurs de charge Ó l'extķrieur de la pile sont des ķlectrons.
1.
Les porteurs de charge Ó l'extķrieur de la pile sont des ķlectrons.
2. Le courant circule du p¶le ┼ de la pile vers le p¶le -
Ó l'extķrieur de la pile. Les ķlectrons circulent en sens opposķ.
2) 1.
couple H+(aq) /H2 (g) :Ā 2 H+(aq) + 2 e-
= H2 (g)
couple O2 (g)/H2O(l):O2 (g)+4H+(aq)+4e-=2H2O(l)
2. Equation :Ā 2 H2 (g) + O2 (g) = 2
H2O(l)
3)
1.Ā Une rķduction est un gain
d'ķlectrons.
Le rķactif qui est rķduit est l'oxydant O2 , c'est le "combustible"
de la pile.
2. L'ķlectrode o∙ se produit la rķduction s'appelle la cathode.
Elle reńoit les ķlectrons, c'est donc le p¶le ┼.
4)
1. n(H2) = m(H2) / M(H2) = 1 500 /
2,0 = 750 molĀ ;Ā
V(H2) = n(H2) . Vm = 750 x 24 = 1,8.104
L = 18 m3
2. Les gaz nķcessaires Ó l'utilisation de cette pile occupent trop de place
pour une voiture.
3. Pour occuper moins de place, on peut comprimer ces gaz , augmenter leur
pression jusqu'Ó les obtenir Ó l'ķtat liquide. V= n.R.T/ P , en augmentant
la pression P , on diminue le volume V.
5)
1.ĀĀ I = 200 AĀĀ
;ĀĀ Q = I . t = 200 x 24 x 3600
= 1,73.107 C
2.Ā Q = n(e-).FĀĀ ;Ā n(e-)
= Q / F = 1,73.107 / 96 500 = 179 mol
D'aprĶs la demi-ķquation : 2 H+(aq) + 2 e-
= H2 (g)Ā , n(H2)cons
= n(e-) /2 = 89,5 mol
©Sciences Mont Blanc