Sujet Bac Afrique Juin 2003
Calculatrice autorisée
I ) Les ondes sismiques (9,5 points)
II ) La pile à combustible (2,5 points)
III ) Réactions acido-basiques (4 points)
Afrique Juin 2003 - I ) Les ondes sismiques :
I ) Etude d'un séisme :
Lors d'un séisme, la Terre est mise en mouvement par des ondes de différentes natures qui occasionnent des secousses plus ou moins violentes et destructrices en surface. On distingue :
- les ondes P, les plus rapides, se propageant dans les solides et dans les liquides.
- les ondes S, moins rapides, ne se propageant que dans les solides.
L'enregistrement de ces ondes par des sismographes ŕ la surface de la Terre permettent de déterminer l'épicentre (lieu de naissance de la perturbation).
Les schémas A et B modélisent la progression des ondes sismiques dans une couche terrestre.
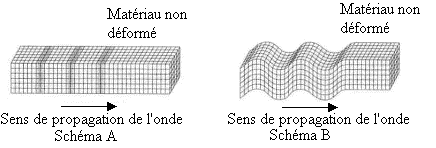
1) Les ondes
P, appelées ondes de compression sont des ondes longitudinales.
Les ondes S, ondes de cisaillement sont des ondes transversales.
a) Définir onde transversale
b) Indiquer le schéma correspondant ŕ chaque type d'onde.
2) Un séisme
s'est produit ŕ San Francisco en 1989.
Le document ci-dessous présente le sismogramme obtenu lors de ce séisme ŕ
la station EUREKA.
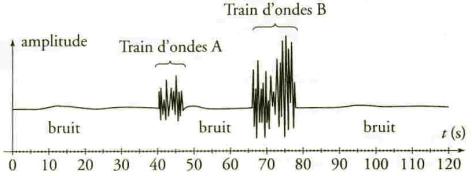
Sismogramme : Station EUREKA
Le
sismogramme a été enregistré ŕ Eureka, station sismique située au nord de
la Californie.
L'origine du repčre (t = 0s) a été choisie ŕ la date du début du séisme ŕ
San Francisco.
a) A quel types d'ondes (S ou P) correspond chaque train ?
Justifier ŕ l'aide du texte d'introduction.
b) Sachant que le début du séisme a été détecté ŕ Eureka ŕ 8h 15min 20s TU
(Temps Universel), déterminer l'heure TU ŕ laquelle le séisme s'est déclenché
ŕ l'épicentre.
c) Sachant que les ondes P se propagent ŕ une célérité moyenne de 10 km.s-1,
calculer la distance séparant l'épicentre du séisme de la station Eureka.
d) Calculer la célérité moyenne des ondes S.
©Sciences Mont Blanc
Afrique Juin 2003 - II ) La pile à combustible :
II ) La pile ŕ combustible :
Le principe des piles ŕ combustible a été découvert par William
Growe en 1839, mais leur utilisation réelle ne date que des années 1960, ŕ
l'occasion des programmes spatiaux de la NASA. Ces piles alimentaient en électricité
les ordinateurs de bord des vaisseaux Gemini et Apollo et fournissaient l'eau
de consommation. En effet, par comparaison aux piles salines et alcalines,
les piles ŕ combustible, type hydrogčne-oxygčne présentent deux avantages
: faire appel ŕ des réactifs (dioxygčne de l'air et dihydrogčne) disponibles
en grande quantité et ętre non polluantes car libérant de l'eau.
Le principe de fonctionnement est simple : la cellule de réaction est composée
de deux électrodes séparées par un électrolyte (exemple : l'acide phosphorique
H3PO4). Elle est alimentée en dihydrogčne et en dioxygčne
en continu. Le fonctionnement de la pile repose sur une réaction d'oxydo-réduction
au niveau des électrodes.
Données : MH = 1,0 g.mol-1 ; MO
= 16,0 g.mol-1; Constante d'Avogadro : NA = 6,02 1023 mol-1 ;
Charge électrique élémentaire : e = 1,6 10-19 C ; Faraday
: 1 F = 96500 C.mol-1
I ) Schéma de la pile ŕ combustible :
1) Quel est la nature des porteurs de charges ŕ l'extérieur de la pile ?
2) Légender
le schéma de la pile ci-aprčs en indiquant le sens conventionnel de circulation
du courant électrique I et le sens de circulation des porteurs de charges
ŕ l'extérieur de la pile.
(en ajoutant des flčches bien orientée) (ŕ rendre avec la copie).
Schéma de la pile ŕ combustible

II ) Les couples d'oxydoréduction mis en jeu dans la réaction sont : H+(aq) / H2 (g) et O2 (g) / H2O (l).
1) Ecrire les demi-équations électroniques pour chaque couple quand la pile débite.
2) En déduire l'équation de la réaction modélisant la transformation ayant eu lieu dans la cellule de réaction.
III ) Le réactif qui est réduit est appelé le "combustible" de la pile.
1) Parmi les espčces chimiques présentes dans les couples, laquelle constitue le combustible ? Justifier la réponse en définissant la réaction de réduction.
2) Préciser le nom de l'électrode oů se produit la réduction. Cette électrode est-elle le pôle positif ou négatif de la pile ?
IV ) Dans un véhicule motorisé fonctionnant grâce ŕ une pile ŕ combustible, on estime ŕ 1,5 kg la masse de dihydrogčne nécessaire pour parcourir 250 km.
1) Calculer la quantité de matičre de dihydrogčne n(H2) correspondant ŕ cette masse, puis le volume de dihydrogčne V(H2) en mčtre-cube (m3) si le volume molaire Vm =24 L.mol-1
2) Justifier le fait que les piles ŕ combustible ne soient pas encore utilisées dans les voitures, en utilisant la réponse ŕ la question IV ) 1).
3) Rappelons
la loi des gaz parfaits : P.V = n.R.T avec :
P (pression du gaz) ; V (volume du gaz) ; n (quantité de matičre du gaz) ;
R ( constante des gaz parfaits) ; T (température du gaz)
Proposer un moyen de réduire l'espace occupé par ce gaz, ŕ température ambiante
pour la quantité de matičre n de gaz calculée précédemment. Justifier ŕ l'aide
de la loi précédente.
V ) Dans la navette spatiale, les piles ŕ combustible débitent un courant d'intensité I=200 A.
1) Calculer la charge électrique Q libérée en 24 heures.
2) En déduire la quantité de matičre nP des porteurs de charge, ayant circulé dans le circuit de la navette pendant 24 heures et la quantité de matičre n(H2) de dihydrogčne consommée.
©Sciences Mont Blanc
Afrique Juin 2003 - III ) Réactions acido-basiques
:
I ) Identification d'un indicateur coloré :
On dispose d'un flacon d'indicateur coloré avec comme seule indication sa concentration molaire C0 = 2,90.10-4 mol.L-1 . On mesure son pH : 4,18.
ON en déduit la concentration molaire en ions oxonium [ H3O+ ] = 6,6.10-5 mol.L-1
Le couple acide/base présent dans cet indicateur coloré sera noté HInd / Ind- .
La solution d'indicateur coloré a été préparé ŕ partir de la forme acide de l'indicateur HInd .
L'équation de la réaction entre HInd et l'eau est : HInd + H2O = Ind- + H3O+
1) En considérant un volume V = 100 mL de solution d'indicateur, déterminer le taux d'avancement final de la réaction de l'acide HInd avec l'eau.
Cet acide est-il totalement dissocié dans l'eau? Justifier votre réponse.
2) Donner l'expression littérale de la constante d'acidité KA de la réaction de l'acide HInd sur l'eau.
3) Les concentrations ŕ l'équilibre permettent de calculer la constante d'acidité de la réaction :
KA = 1,9.10-5 Sachant que pKA = -log KA ; calculer le pKA du couple Hlnd/lnd- et identifier l'indicateur ŕ l'aide des données du tableau suivant :
|
Indicateur |
Couleur acide |
Zone de virage |
Couleur basique |
pKA |
|
Héliantine |
jaune orangé |
3,1 - 4,4 |
rouge |
3,7 |
|
Vert de bromocrésol |
jaune |
3,8 - 5,4 |
bleu |
4,7 |
|
Bleu de bromothymol |
jaune |
6,0 - 7,6 |
bleu |
7,0 |
|
Phénolphtaléine |
incolore |
8,2 - 10,0 |
fuschia |
9,4 |
II ) Dosage d'une solution d'acide chlorhydrique concentrée :
Dans le laboratoire d'un lycée, on dispose d'un flacon d'une solution d'acide chlorhydrique concentrée oů est notée sur l'étiquette l'indication suivante:
33 % minimum en masse d'acide chlorhydrique
On appellera cette solution S0 . On veut connaître la concentration molaire C0 de cette solution. Premičre étape : On dilue 1 000 fois la solution S0. On obtient alors une solution S1 de concentration C1.
Deuxičme étape : On prélčve précisément un volume V1 = 100,0 mL de solution S1
On dose par conductimétrie la solution S1 par une solution titrante d'hydroxyde de sodium de concentration CB = 1,00.10-1 mol.L-1 . La représentation graphique de la conductance de la solution en fonction du volume V de solution titrante versé est donnée dans l'annexe, document 1.
1) On ajoute la solution d'hydroxyde de sodium pour
doser la solution S1
Ecrire l'équation de la réaction acido-basique.
2) Déterminer graphiquement, sur le document 1 de l'annexe, le volume versé VE ŕ l'équivalence. 3) A l'équivalence, écrire la relation existant entre C1 , CB, VE et V1 et calculer la concentration molaire C1 de la solution d'acide chlorhydrique diluée S1
4) En déduire la concentration molaire C0 de la solution d'acide chlorhydrique concentrée S0 .
5) Calculer la masse m0 d'acide chlorhydrique HCl dissous dans un litre de solution.
Donnée : Masse molaire de l'acide chlorhydrique
M(HCl) = 36,5 g.mol-1 .
La solution S0 a une masse volumique r0 = 1 160 g.L-1. Le pourcentage
massique de la solution S0 représente la masse d'acide chlorhydrique
dissous dans 100 g de solution.
6) Quelle est la masse m d'un litre de solution S0 ?
7) Calculer le pourcentage massique de la solution S0 . L'indication de l'étiquette du flacon de solution d'acide chlorhydrique concentrée est-elle correcte?
Une simulation du dosage par suivi pH-métrique de la solution S1 est donnée dans l'annexe, document n°2.
8) Sur le document n° 2, indiquer la zone de virage de l'indicateur
identifié ŕ la question I.3)
En utilisant cet indicateur pour le dosage de la solution S1 ,
décrire le changement de couleur observé.
9) Dans la liste donnée ŕ la question I.3), y-a-t-il un indicateur coloré mieux adapté pour repérer l'équivalence du dosage? Justifiez votre réponse.
Annexe: ŕ rendre avec la copie
Dosage de la solution diluée d'acide chlorhydrique S1 par conductimétrie
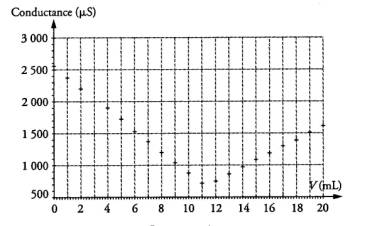
document 1
©Sciences Mont Blanc