Sujet Bac Asie Juin 2003
Calculatrice autorisée
I ) Fabrication et propriétés d'un savon (4 points)
II ) Les applications technologiques de la radioactivité (6,5 points)
III ) QROC : A propos de l'énergie (5,5 points)
I ) (spe) Dosage d'une eau de Javel (4 points)
Asie Juin 2003 - I ) Fabrication et propriétés d'un savon :
©Sciences Mont Blanc
Asie Juin 2003 - II ) Les applications technologiques de la radioactivité :
Document : Médecine et radioactivité :
Au cours du XXe sičcle, d'énormes progrčs ont été réalisés en médecine grâce ŕ la radioactivité. La technique consiste ŕ introduire dans l'organisme des substances radioactives appelées traceurs pour diagnostiquer (identifier la maladie) et soigner. Par exemple, on sait que les phosphonates entrent dans le métabolisme* osseux : si on injecte du phosphonate radiomarqué au "technétium 99", celui-ci se comporte comme un traceur. Il participe au métabolisme de la męme façon que le phosphonate naturel auquel il est mélangé et se répartit sur le squelette. Le rayonnement gamma émis traverse les tissus et peut donc ętre détecté ŕ l'extérieur de l'organisme par une gamma caméra. Cette caméra permet d'obtenir des informations sous forme d'une image appelée la scintigraphie. Celle-ci pourra apporter des renseignements fonctionnels comme, par exemple, le degré de consolidation d'une fracture.
D'autres traceurs sont utilisés; citons: l' "iode 131"; le "carbone 11"; l' "azote 13"; l' "oxygčne 15". Ils sont choisis parce que leur activité décroît rapidement.
La radioactivité est utilisée dans le traitement des tumeurs et des cancers : c'est la radiothérapie. Le principe consiste ŕ bombarder une tumeur avec le rayonnement b- émis par le "cobalt 60".
Dans certains cas, il faut une source radioactive plus ionisante : on utilise un rayonnement de type alpha, plus massif que les autres.
La découverte de la radioactivité a donné aux sciences, ŕ la médecine et ŕ l'industrie un élan qui, aprčs un sičcle, ne s'est pas ralenti."
* Le métabolisme représente l'ensemble des transformations physiques et chimiques dans les tissus vivants.
A) Questions préalables
1)
Par quels nombres caractérise-t-on le noyau d'un atome ?
2) Le "carbone 11" et le "carbone 12" sont deux isotopes.
Qu'est-ce qui différencie les isotopes d'un męme élément chimique ?
3) L' "oxygčne 15" est radioactif b+.
Ecrire l'équation de la désintégration correspondante.
On supposera que le noyau fils n'est pas émis dans un état excité.
Extrait de la classification périodique :
|
6C |
7N |
8O |
9F |
10Ne |
11Na |
B)
A propos du texte
1) Dans le texte on parle de traceurs, quelle propriété commune présentent-ils?
2) Le texte donne une particularité des radioéléments utilisables en scintigraphie,
laquelle?
3) Quelques types de rayonnement :
a) Dans le texte, il est question de radioactivité b- et a ; donner le nom et le symbole ![]() de
chacune de ces particules.
de
chacune de ces particules.
b) Justifier ŕ partir de la question précédente la phrase "un rayonnement
de type alpha plus massif que les autres".
C) Scintigraphie :
On injecte ŕ un patient un échantillon d' "iode 131" de temps de
demi-vie égal ŕ 8 jours environ.
1) Donner la définition du temps de demi-vie.
2) En vous aidant du tableau ci-dessous, justifier le choix de l' "iode
131" en scintigraphie.
|
|
Activité A0
(en Bq) |
Activité A400
(en Bq) |
|
traceur de demi-vie
égale |
2.105 |
6.10-3 |
|
traceur de demi-vie
égale |
2.105 |
6 255 |
D)
Radiothérapie :
Le cobalt ![]() est
émetteur b- de constante
radioactive l = 4.10-9
s-1.
est
émetteur b- de constante
radioactive l = 4.10-9
s-1.
1) Ecrire l'équation de désintégration du "cobalt 60". On supposera
que le noyau fils est produit dans un état excité.
Données :
Extrait de la classification périodique :
|
25Mn |
26Fe |
27Co |
28Ni |
29Cu |
Constante
d'Avogadro: 6,02.1023 mol-1
Masse molaire atomique du cobalt 60 : 60 g.mol-1.
2) Un centre hospitalier reçoit un échantillon de "cobalt 60".
a) Déterminer le nombre N0 de noyaux contenus dans l'échantillon
de 1µg ŕ l'instant de sa réception dans l'établissement hospitalier.
b) Rappeler l'expression liant DN,
Dt, l
et N dans laquelle N représente le nombre de noyaux encore présents dans l'échantillon
ŕ l'instant de date t.
c) Donner l'expression de DN en fonction
de Dt, l, N0 et t.
Le technicien du laboratoire est chargé de contrôler cette source, tous les
ans, pendant 10 ans.
A l'aide d'un compteur, il détermine le nombre de désintégrations DN obtenues pendant une courte durée notée Dt = 1 s. Ce nombre est appelé activité A définie
par |DN|/ Dt.
d) Montrer que l'activité A= |DN|/
Dt peut
se mettre sous la forme A = A0.e-l.t.
Que vaut littéralement A0?
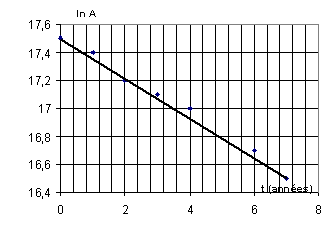 e)
On trace ŕ l'aide d'un logiciel approprié le graphe du logarithme de l'activité
A en fonction du temps :
e)
On trace ŕ l'aide d'un logiciel approprié le graphe du logarithme de l'activité
A en fonction du temps :
ln A = f (t).
On
rappelle que : ln(ab) = ln a + ln b
Exprimer ln A en fonction de t, l
et A0 , activité initiale de l'échantillon ŕ l'instant de sa réception
.
f)
Montrer que la forme de la courbe ci-dessus constitue une vérification expérimentale
de l'expression trouvée précédemment.
g) Déterminer graphiquement la valeur de la constante de désintégration radioactive
l en an-1.
h) Donner la relation entre t1/2 et l.
i) Calculer t1/2 en années. Dans les tables on trouve t1/2
=1,68.108s pour le "cobalt 60".Commenter.
©Sciences Mont Blanc
Asie Juin 2003 - III ) QROC : A propos de l'énergie
:
Cet exercice est un Questionnaire ŕ Réponses Ouvertes et Courtes.
A chaque affirmation, vous répondrez par VRAI ou FAUX.
Toute réponse doit ętre accompagnée de justifications ou de commentaires brefs (définitions, calculs, exemples ou contre-exemples ...).
Question 1
On a réalisé le montage ci-dessous avec les composants suivants : un conducteur ohmique de résistance R = 4,0. 102 W, une bobine d’inductance L = 0,40 H (résistance interne de la bobine négligée) et un condensateur de capacité C = 1,0.10-6 F.
On charge le condensateur, commutateur basculé en position 1, puis, ŕ l’instant de date t0 = 0, le commutateur est basculé en position 2.
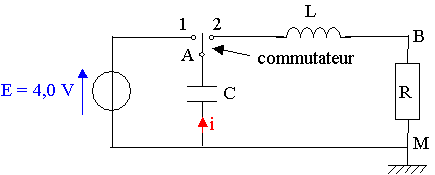
Les points A, B et M sont reliés ŕ un ordinateur ou ŕ un systčme d’acquisition. Grâce ŕ un logiciel adapté on observe l’évolution des tensions au cours du temps (schéma ci-aprčs).
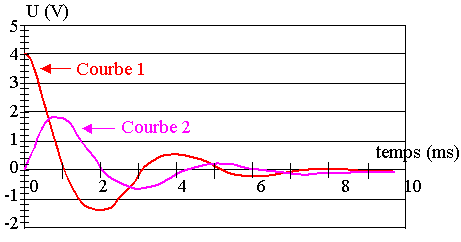
1) A propos des courbes
La courbe 1 visualisée est :
a. la tension aux bornes du condensateur
b. la tension aux bornes du conducteur ohmique
c. la tension aux bornes de la bobine
La courbe 2 visualisée est :
d. la tension aux bornes de la bobine
e. la tension aux bornes du conducteur ohmique
2) A propos des énergies
A l’instant initial le circuit RLC a emmagasiné une énergie E1 de :
a. 8,0 mJ b. 8,0.10-6 J c. 2,0. 10-6 J
3) Lorsque les deux courbes se coupent pour la premičre fois, la valeur de l’intensité du courant vaut :
a. 5,0 mA b. 7,7 mA c. 4,2 mA
4) Lorsque les deux courbes se coupent pour la premičre fois, la somme des énergies emmagasinée dans la bobine et dans le condensateur notée E2 est :
a. 7,0.10-6 J b. 5,0.10-6 J c. 2,0.10-6 J
5) Lorsque les deux courbes se coupent pour la premičre fois, l’énergie qui a été dissipée dans la résistance vaut :
a. 3,0.10-6 J b. 1,0.10-3 J c. 10 mJ
Question 2
On donne le graphe représentant en fonction du temps l’énergie cinétique et l’énergie potentielle élastique d’un systčme solide–ressort horizontal, écarté de sa position d’équilibre, lâché sans vitesse initiale ŕ l’instant t = 0 s et ŕ l’abscisse x0.
L’origine des abscisses correspond ŕ la position d’équilibre du systčme.
La courbe correspondant ŕ l’énergie cinétique est représentée en trait plein.
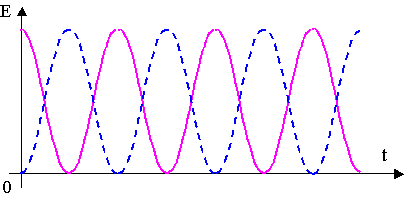
On suppose que l’énergie potentielle de pesanteur est nulle au niveau horizontal oů se situe le systčme. Le systčme de masse m, comporte un ressort de raideur k.
L’expression de l’énergie mécanique du systčme est donnée par l’expression : Em = ˝ k.x02
L’allure des courbes permet d’affirmer qu’il n’y a pas de frottements.
Question 3 :
On dispose d’une solution de nitrate d’argent Ag+(aq) + NO3-(aq) de concentration 0,10 mol.L-1, d’une solution de sulfate de cuivre de concentration 0,50 mol.L-1, d’un fil d’argent, d’une lame de cuivre et d’un pont salin au nitrate de potassium.
On peut former une pile par l’association des couples Ag+(aq) / Ag(s) et Cu2+(aq) / Cu(s).
Soit l’équation de réaction : 2 Ag+(aq) + Cu(s) = 2 Ag(s) + Cu2+(aq)
La constante d’équilibre est K = 2,0.1015.
1) On relie les deux métaux constituant les bornes de la pile par une chaîne conductrice, le quotient de réaction initial de ce systčme, pour l’équation donnée est :
a) Qr, i = 50, alors la réaction est spontanée dans le sens direct.
b) Qr, i = 50, alors la réaction est spontanée dans le sens inverse.
c) Qr, i = 0,02, alors la réaction est spontanée dans le sens direct.
d) Qr, i = 0,02, alors la réaction est spontanée dans le sens inverse.
2) Lorsque cette pile fonctionne (ou débite) son quotient de réaction :
a) augmente.
b) diminue.
c) ne varie pas.
3) Quel est le pôle négatif de la pile :
a) l’électrode d’argent ?
b) l’électrode de cuivre ?
Question 4 :
Une pile de ce type a une f.é.m. E = 2,0 V ; elle est prévue pour fonctionner pendant 10 h si elle débite de maničre constante un courant d’intensité 320 mA.
Données : 1 F = 9,65.104 C.mol-1
1) L’énergie maximale disponible de cette pile est égale ŕ :
a) 11,5 J ;
b) 1,15.104 J ;
c) 2,30.104 J.
2) La quantité d’électrons qui circulent pendant la durée totale du fonctionnement est égale ŕ :
a) 0,12 mol ;
b) 1,0 mol ;
c) 2,0 mol.
©Sciences Mont Blanc
Asie Juin 2003 - I ) (spe) Dosage d'une eau de
Javel :
Document :
Charles Guillaume Scheele, pharmacien suédois, découvrit le dichlore au XVIII sičcle.
Ce gaz intervient dans la fabrication de l'eau de Javel; celle-ci doit son nom ŕ un ancien village qui est aujourd'hui un quartier de Paris. C'est ŕ Javel que Claude Louis Berthollet, directeur ŕ la manufacture des Gobelins, fabriqua ce produit décolorant et désinfectant et l'employa en 1785 au blanchiment des toiles textiles.
L'eau de Javel est obtenue par action du dichlore Cl2(g) sur l'hydroxyde de sodium ou soude et contient des ions Cl-(aq) , ClO-(aq) , Na+(aq) ainsi que H2O(l). C'est donc une solution aqueuse constituée entre autres d'ions chlorure Cl-(aq) et d'ions hypochlorite ClO-(aq).
En milieu acide, l'eau de Javel subit une transformation complčte représentée par la réaction d'équation : Cl-(aq) + ClO-(aq) + 2 H+(aq) = Cl2(g) + H2O(l)
Cette transformation permet de définir le degré chlorométrique. Celui-ci est égal au volume, exprimé en litres, de dichlore produit par un litre d'eau de Javel. Ce volume est mesuré ŕ une température ŕ o °C sous une pression de 1,013 bar.
Pour vérifier l'indication portée sur une bouteille commerciale d'eau de Javel, 12 °chl
(12 degrés chlorométriques), on réalise un titrage.
Principe de la manipulation :
On ajoute un excčs d'ions iodure ŕ un volume connu de solution d'eau de Javel. Les ions hypochlorite ClO-(aq) oxydent en milieu acide les ions iodure I-(aq) .
L'équation de la réaction modélisant la transformation est :
ClO-(aq) + 2 I-(aq) + 2 H+(aq) = I2 (aq) + Cl-(aq) + H2O(l) (1)
On considérera cette réaction comme totale.
Le diode formé appartenant au couple I2 (aq) / I-(aq) est titré par les ions thiosulfate, réducteurs du couple S4O62-(aq) / S2O32-(aq) . On en déduit alors la quantité d'ions hypochlorite, puis le degré chlorométrique.
I ) Mode opératoire :
1) L'eau de Javel commerciale étant trop concentrée, il faut d'abord effectuer une dilution au dixičme pour obtenir 50,0 mL de solution diluée S. Décrire une méthode qui permet d'effectuer cette dilution. On précisera la verrerie nécessaire (noms et volumes).
2) Dans un erlenmeyer, on introduit dans cet ordre :
- V= 10,0 mL de solution S ;
- V' = 20 mL de la solution d'iodure de potassium (K+(aq) + I-(aq) ).
Quelle verrerie faut-il utiliser pour prélever les volumes :
- V= 10,0 mL de solution S ?
- V' = 20 mL de solution d'iodure de potassium ?
II ) Titrage :
A l'aide d'une solution du thiosulfate de sodium de formule ( 2 Na+(aq) + S2O32-(aq)) de concentration molaire apportée c1 = 0,10 mol.L-1 , on titre le diode formé. On ajoure une pointe de spatule de thiodčne afin de mieux repérer l'équivalence.
Le volume équivalent est V1E = 10,0 mL.
1) Ecrire l'équation de la réaction de titrage qui sera notée (2), entre le diode et les ions thiosulfate.
2) Déduire des résultats du titrage la quantité de matičre de diiode présente dans le mélange réactionnel.
Cette quantité de matičre correspond aussi ŕ la quantité produite lors de la réaction (1).
3) Calculer la quantité de matičre d'ions hypochlorite initialement présents dans le prélčvement de volume V.
4) Déterminer la concentration en ions hypochlorite de la solution S, puis de la solution commerciale.
5) a) En utilisant l'équation de la réaction chimique donnée dans le document, calculer la quantité de matičre de dichlore produite par un litre d'eau de Javel.
b) Le volume molaire d'un gaz parfait, dans les conditions de température et de pression citées dans le texte, vaut 22,4 L.mol-1 .
En déduire le degré chlorométrique de l'eau de Javel commerciale utilisée. Commenter le résultat.
©Sciences Mont Blanc
