Correction Bac Liban Juin 2003
Calculatrice autorisée
I – Evolution temporelle de deux oscillateurs (9 points)
II - Pile cuivre-argent (3 points)
III – Etude de l'estérification (4 points)
Correction Liban Juin 2003 - I ) Evolution temporelle de
deux oscillateurs
A ) Oscillateur mécanique :
1)
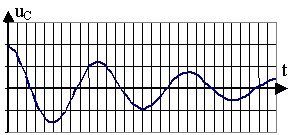
L'enregistrement 3 correspond ŕ des oscillations non amorties, il est
donc obtenu dans le cas a) soufflerie ŕ puissance maximale. Le régime est
périodique.
L'enregistrement 1 correspond ŕ des oscillations amorties faibles, il est
donc obtenu dans le cas b) puissance de la soufflerie légčrement diminuée.
Le régime est pseudo-périodique.
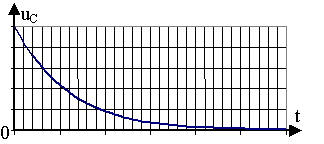
L'enregistrement 2 correspond ŕ des oscillations fortement amorties, il est
donc obtenu dans le cas c) puissance de la soufflerie fortement diminuée.
Le régime est apériodique.
2)
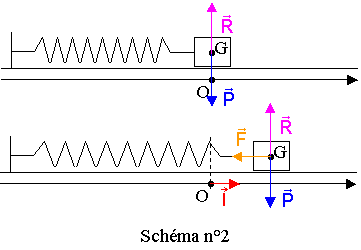 a)
forces exercées sur le solide S :
a)
forces exercées sur le solide S :
R
: réaction normale du plan
P
: poids du solide S
F
: force de rappel du ressort
b) On applique la 2čme loi de Newton dans le référentiel
terrestre galiléen,
au systčme solide S : P + R
+ F
= m. a
G
Projection sur l'axe Ox : 0 + 0 + Fx = m.a x (1)
Fx = - k.x Ţ (1) – k.x = m.x'' = m.d2x/dt2
Ţ m. d2x/dt2 + k.x = 0
c) x = XM.cos(2 p t / T0 + F0) ; XM
est l'amplitude et F0 est la phase
ŕ l'origine.
ŕ t = 0 s , vx = 0 m.s-1 et x = 10,0 cm ; x = XM.cos F0
= x0
vx = dx/dt = - (2 p / T0) . XM.sin(2 p t /
T0 + F0) ;
 |
ŕ t = 0 s , dx/dt = - ( 2 p / T0).XM.sin F0 = 0 Ţ sin F0 = 0 Ţ F0 = 0 ou p
Si F0 = 0 , x0 = XM et si F0 = p , x0 = - XM ce qui est impossible car x0 > 0
Ţ F0 = 0 ; x0 = XM = 10,0 cm = 0,1 m ; x = x0.cos(2 p t / T0)
d) On utilise l'enregistrement 3 car les frottements sont
négligeables et les oscillations sont non amorties.
D'aprčs l'enregistrement 3, une période T0 vaut 1 s.
e) étudions les différentes propositions.
F = k. ˝x˝ ; [
k ] = [ F / ˝x˝] =
[m.a / ˝x˝] =
M.L.S-2 / L= M.S-2
[2 p ![]() ( m / k )] = [ m / k ]1/
2 = M1/ 2 .(M.S-2)-1/
2 = M1/ 2 .M-1/ 2 .S1 = S1
( m / k )] = [ m / k ]1/
2 = M1/ 2 .(M.S-2)-1/
2 = M1/ 2 .M-1/ 2 .S1 = S1
ceci est compatible avec un temps comme la période T0 .
[2 p![]() (
k / m )] = [ k / m ]1/ 2 =(M.S-2)1/
2 . M-1/ 2 = M1/ 2 . .S-1 .
M-1/ 2 = S-1
(
k / m )] = [ k / m ]1/ 2 =(M.S-2)1/
2 . M-1/ 2 = M1/ 2 . .S-1 .
M-1/ 2 = S-1
ceci est compatible avec l'inverse d'un temps . Cette formule est donc fausse
.
[2 p m / k] = [ m / k ] = M .(M.S-2)-1
= M.M-1.S2 = S2
ceci est compatible avec un temps au carré. Cette formule est donc fausse.
T0
= 2p![]() (
m / k ) Ţ T02
/ 4 p2= m / k Ţ k = m.4 p2/ T02 = 0,1 x 4 x 3,142 / 1,02
= 3,95 N.m-1
(
m / k ) Ţ T02
/ 4 p2= m / k Ţ k = m.4 p2/ T02 = 0,1 x 4 x 3,142 / 1,02
= 3,95 N.m-1
3) a) Ep
élast. = ˝ k.x2 ;
Ec = ˝ m.v2 ; E
= Ep + Ec
b) ŕ t = 0 s , x = XM ;
v = 0 m.s-1 ; E
= ˝ k.x2 + ˝ m.v2 = ˝ k.XM2 =
˝ x 3,95 x 0,12 = 0,02 J
Au cours du mouvement , l'énergie mécanique E se converse, elle est constante. E = 0,02 J
A la position d'équilibre, x = 0 m, Ep = 0 J , E
= Ec = ˝ m.v2
v = ![]() ( 2 E / m ) =
( 2 E / m ) = ![]() ( 2 x 0,02 / 0,1) = 0,63
m.s-1
( 2 x 0,02 / 0,1) = 0,63
m.s-1
c)
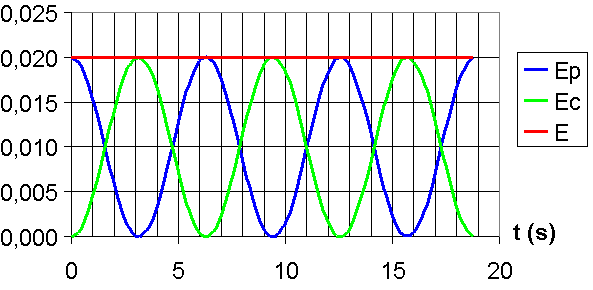 |
On détermine facilement la courbe correspondante ŕ l'énergie E car elle est constante.
Ensuite, on connaît les valeurs ŕ t = 0 s , Ec = 0 J et Ep
= E = 0,02 J.
Cela permet de distinguer les 2 autres courbes.
d) Dans un régime pseudo-périodique, l'énergie mécanique diminue car il y a de l'énergie dissipée par frottements.
B ) Application des oscillations électrique :
1)
|
Si la résistance R est faible, l'amortissement est faible, le régime est pseudo-périodique. |
Si la résistance R est grande, l'amortissement est important , le régime est apériodique. |
|
|
|
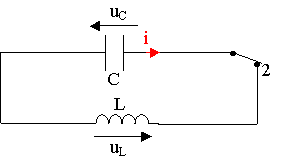 2)
R = 0 W. Elle disparaît du montage.
2)
R = 0 W. Elle disparaît du montage.
On choisit un sens de courant et on flčche les tensions en respectant la convention récepteur.
Loi des tensions dans le circuit : uC + uL = 0 (1)
q = C.uC ; i = dq/dt ; uL = L.di/dt = L.d2q/dt2
On remplace dans la relation (1) :
q /C + L.d2q/dt2 = 0 ou q + LC.d2q/dt2 = 0 (2)
3) q = QM.cos(2p.t / T0 + f0 ) ; dq/dt = - QM.(2p / T0).sin(2p.t / T0 + f0 )
d2q/dt2 = - QM.(2p / T0)2 .cos(2p.t / T0 + f0 ) . On remplace dans la relation (2).
(2) QM.cos(2p.t / T0 + f0 ) - L.C.QM.(2p / T0)2 .cos(2p.t / T0 + f0 ) = 0
(2) QM.cos(2p.t / T0 + f0 ).[ 1 - L.C.(2p / T0)2 ] = 0
Pour que la relation (2) soit valable quelque soit l'intant t , il faut : 1 - L.C.(2p / T0)2 = 0
(2p / T0)2 = 1 / (L.C) Ţ T0 /
2p
= ![]() (L.C)
Ţ T0 = 2p.
(L.C)
Ţ T0 = 2p.![]() (L.C)
(L.C)
L'expression proposée est bien une solution de l'équation
différentielle avec T0 = 2p.![]() (L.C).
(L.C).
4) T = 31,4 ms ; L = 200 mH ; T2 = 4p2.L.C Ţ C =T2 / ( 4 p2.L )
C = (31,4.10-6)2 / (4 x 3,142.200.10-3 ) = 1,25.10-10 F = 125 pF
5) a) C = a.h + b Pour cette relation, on choisit C en pF pour simplifier l'expression.
D'aprčs les caractéristiques du capteur, si h varie de 1 %, la capacité C varie de 0,4 pF
DC = a.Dh Ţ a = DC / Dh = 0,4 / 1 = 0,4 ;
si h = 43 % d'HR , C = 122 pF = 43 a + b = 0,4 x 43 + b Ţ b = 122 - 0,4 x 43 = 104,8
Si C est en pF , on a : C = 0,4 h +104,8
b) Dans l'expérience , la capacité C vaut 125 pF .
C = 0,4 h + 104,8 Ţ h = (C - 104,8 ) / 0,4 = (125 -104,8 ) / 0,4 = 50,5 % d'HR
©Sciences Mont Blanc
Correction Liban Juin 2003 - II ) Pile cuivre-argent
A) Transformation chimique spontanée par transfert direct d'électrons :
1) L'intensification de la coloration bleue indique la formation d'ions Cu2+ et le dépôt gris correspond ŕ du métal Argent formé. IL s'agit donc de la réaction (1).
2) Critčre d'évolution spontanée : Si Qr,i < K , l'évolution est dans le sens direct et si Qr,i > K , l'évolution se fait en sens opposé .
3)
Equation : Cu(s) + 2Ag+(aq) = Cu2+(aq)
+ 2Ag(s)
Qr,i = [Cu2+]i / [Ag+ ]i2
= (C1/2) / (C2/2)2 = 0,5 / 0,252
= 8
Qr,i < K1 , le systčme évolue dans le sens direct.
Ceci est compatible avec les observations puisqu'on observe la formation des
ions Cu2+ et de métal argent.
B) Constitution et fonctionnement de la pile cuivre-argent en circuit fermé
1)
 Schéma
Schéma
2) a) Le courant circule de l'électrode d'argent vers l'électrode
de cuivre, et sort du pôle Ĺ, qui est donc l'électrode
d'argent, le pôle - est donc l'électrode
de cuivre.
b) A l'électrode de cuivre : Cu(s) = Cu2+(aq)
+ 2 e-
A l'électrode d'argent : Ag+(aq)
+ e- = Ag(s)
c) Equation : Cu(s) + 2Ag+(aq) = Cu2+(aq) + 2Ag(s)
d) Si le systčme était en équilibre, il n'y aurait pas circulation d'électrons, pour que la pile fonctionne, il faut que Qr,i ą K. Le systčme est hors équilibre.
©Sciences Mont Blanc
Correction Liban Juin 2003 III ) Etude de l'estérification
:
n(ethanol)0 =0,10 mol ; n(ac.eth)0 = 0,10 mol
1) CH3–CH2–OH + CH3–COOH = CH3–COO–CH2–CH3 + H2O
L'ester est l'éthanoate d'éthyle
2) On refroidit rapidement les ampoules avant chaque dosage pour stopper l'estérification.
3) a)
|
Equation de la réaction |
C2H5–OH+CH3–COOH = CH3–COO–C2H5+H2O |
||||
|
Etat du systčme |
Avancement |
Quantité de matičre en mol |
|||
|
Etat initial |
0 |
0,10 |
0,10 |
0 |
0 |
|
en cours |
x |
0,10 - x |
0,10 - x |
x |
x |
|
Etat final |
xf |
0,10 – xf |
0,10 – xf |
xf |
xf |
Si la réaction est totale, n(éthanol)f = 0 = n(ethanol)0 – xmax ;
xmax = n(ethanol)0 = 0,10 mol = 100 mmol ( ou męme raisonnement avec l'acide éthanoďque )
b) D'aprčs le tableau, n(CH3–COOH)f = 100 – xf Ţ xf = 100 – n (en mmol)
4) t = xf / xmax
|
Date t (en h) |
0 |
4 |
10 |
20 |
40 |
100 |
150 |
200 |
250 |
300 |
|
Quantité de matičre n (mmol) |
100 |
75 |
64 |
52 |
44 |
36 |
35 |
34 |
33 |
33 |
|
Avancement final xf (mmol) |
0 |
25 |
36 |
48 |
56 |
64 |
65 |
66 |
67 |
67 |
|
taux d'avancement t |
0 |
0,25 |
0,36 |
0,48 |
0,56 |
0,64 |
0,65 |
0,66 |
0,67 |
0,67 |
5)
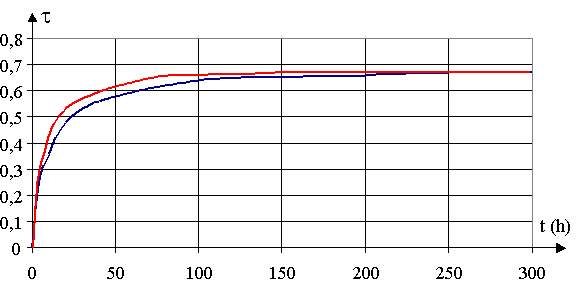 |
La courbe rouge est celle correspondant ŕ une température plus élevée.
6) La courbe montre que la transformation est lente et limitée par l'hydrolyse de l'ester ( xf < 1 )
7) Si on augmente la température, la transformation est plus rapide mais l'état d'équilibre n'est pas modifié, tf reste ŕ 0,67 . La température est un facteur cinétique.
©Sciences Mont Blanc