Correction Bac Réunion Juin 2004
Calculatrice autorisée
I ) Quelques usages des condensateurs (9 points)
II ) QROC : A propos de l'électrolyse (3 points)
III ) La catalyse homogène
(4 points)
I ) (spe) Détermination du degré
alcoolique d'un vin (4 points)
Correction Réunion Juin 2004 - I ) Quelques usages
des condensateurs :
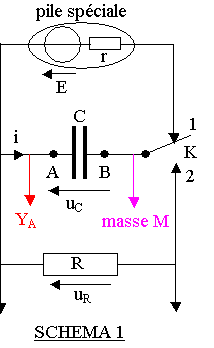 I ) Génération d'impulsions
: le stimulateur cardiaque
I ) Génération d'impulsions
: le stimulateur cardiaque
1) Charge du condensateur :
a) Ce phénomčne est trčs rapide car dans ce circuit , la seule résistance est la résistance interne r de la pile qui est trčs faible.
t = r.C. La constante de temps t est donc trčs faible.
Cela indique que la charge du condensateur est trčs rapide.
b) voir schéma ci-contre.
c) Lors de la charge, la tension uC augmente en fonction du temps.
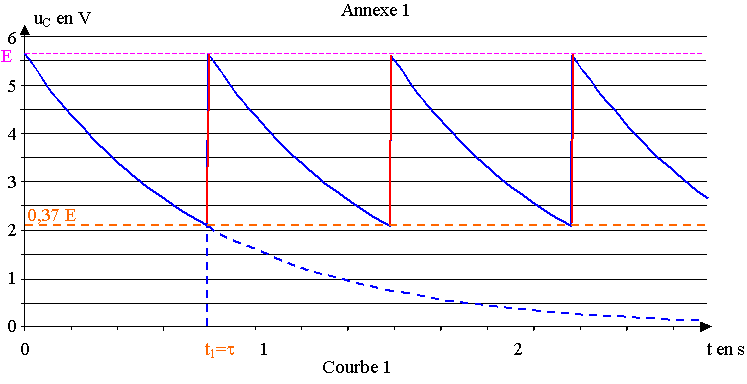
Sur la courbe 1, les parties coloriées en rouge correspondent ŕ la charge.
d) Lorsque le condensateur est complčtement chargé, tous les électrons disponibles de l'armature A du condensateur sont partis vers l'autre armature B, il n'y a plus de circulation d'électrons, l'intensité du courant qui circule dans le circuit est nulle. i = 0 A.
D'aprčs la courbe 1, E vaut environ 5,6 V.
2) Décharge du condensateur :
a) En respectant les conventions d'orientations du schéma du circuit :
Lors de la charge, les électrons se sont accumulées sur l'armature B, lors de la décharge, ils repartent vers l'armature A dans le circuit de décharge.
L'intensité i du courant lors de la décharge est négative.
Relation entre l'intensité i du courant et la tension uR :
uR et i sont de męme sens, cela ne respecte pas la convention récepteur. uR = - R.i
Relation entre la charge q de l'armature A du condensateur et la tension uC :
qA > 0 car les électrons s'accumulent sur l'armature B.
qA = C.uC
Relation entre l'intensité i et la charge q : i = dq/dt
Relation entre les tensions uR et uC lors de la décharge :
D'aprčs la loi des mailles en partant de B vers la gauche : uC - uR = 0 (1)
b) uR = - R.i = - R.dq/dt = - R.C.duC/dt
En remplaçant dans la relation (1), on a : uC + R.C.duC/dt = 0
En divisant par t = R.C , on obtient : uC / t + duC/dt = 0 (2)
c) t = R.C.
Analyse dimensionnelle : [R.C] = [R].[C]
[R] = [uR / i ] = U / I ( U : dimension d'une tension, I : dimension d'une intensité)
Dans le cours sur les piles, q = i . t . [q] = I.T , [C] = [q / uC ] = I.T / U
[R.C] = [R].[C] = (U / I ) . (I . T / U) = T
Le produit R.C est donc homogčne ŕ une durée dont l'unité est la seconde.
d) ŕ t = t, uC(t) = 0,37 E = 0,37 x 5,6 = 2,1 V.
D'aprčs la courbe 1, t correspond ŕ t1, soit 0,8 s.
e) t = R.C. Ţ R = t / C = 0,8 / 470.10-9 = 1,7.106 W = 1,7 MW
3) Lien entre la décharge du condensateur et les battements du cśur :
a) D'aprčs l'énoncé, uC (t1) = E / e
Ceci est en accord avec la question d. E / e = 0,37 E = 2,1 V
b) uC(t) = E.e- t / t = E.e-1 = E / e. On a donc t1 = t
c) D'aprčs la courbe 1, la tension uC(t) décroît lors de la décharge jusqu'ŕ E/e en un temps t.
La durée Dt qui doit séparer deux impulsions électriques consécutives doit donc correspondre ŕ t.
d) N : nombre de battements du cśur par minute . N = 60 / t = 60 / 0,8 = 75
II ) Stockage d'énergie : le flash électronique
1) D'aprčs les données du mode d'emploi, la valeur de l'énergie libérée par un éclair d'intensité lumineuse et de durée maximales vaut 90 J ((18000 /2) pour 100 éclairs, soit 90 J par éclair).
2) EC = ˝ C.U2 Ţ C = 2 EC / U2 = 2 x 90 / 62 = 5 F
3) D'aprčs les données du mode d'emploi, le temps maximum de recharge vaut 11 s.
Le condensateur est rechargé ŕ 99 % pour t = 5 t.
L'ordre de grandeur de la constante de temps t du circuit de charge pour un éclair d'intensité lumineuse et de durée maximales est de 2 s.
4) t = R.C Ţ R = t / C = 2 / 5 = 0,4 W
L'ordre de grandeur de la résistance ŕ travers laquelle s'est chargé le condensateur est 0,4 W.
III ) Oscillations électriques : le détecteur de fraude
T0 = 1 / N = 1,0.10-7 s. T02 = 4 p2.L.C
Ţ C = T02 /(4 p2.L) = (1,0.10-7)2 /(4 x 3,142 x 0,5.10-6) = 5.10-10 F = 0,5 nF
©Sciences Mont Blanc
Correction Réunion Juin 2004 - II ) QROC
: A propos de l'électrolyse :
I ) Dans l'industrie monétaire, on cuivre une rondelle d'acier appelée flan pour obtenir certaines pičces de monnaie comme les pičces de 1, 2 et 5 centimes d'euros.
1) L'électrolyse est une transformation chimique forcée car elle s'effectue
en sens inverse du sens de la transformation spontanée.
2) La demi-équation électronique modélisant la réaction qui a lieu au niveau de la rondelle métallique est Cu2+(aq) + 2 e- = Cu (S) car il faut que du métal cuivre soit formé et déposé dessus.
3) Cette rondelle est reliée ŕ la borne - du générateur de tension continue car les électrons sortent de cette borne et arrivent ŕ la rondelle pour réagir avec les ions Cu2+ de la solution.
4) Ce « flan » constitue la cathode de l'électrolyseur car il s'y produit la réduction qui est toujours cathodique.
5) Pour maintenir constante la concentration en ions cuivre II ( Cu2+) dans l'électrolyte, on place une électrode de cuivre ŕ l'anode pour y produire l'oxydation du métal cuivre en ions Cu2+ .
II ) En fait, le cuivrage s'effectue, ŕ 60°C, sur un tonneau dans lequel peut se trouver 80 kg de rondelles d'acier, soit environ 18000 rondelles.
1) La masse de cuivre ŕ déposer, sur une rondelle d'acier, est de :
V = S . e = 9,2.10-4 x 25.10-6 = 2,3.10-8 m3
m = r . V = 8960 x 2,3.10-8 = 2,06.10-4 kg = 0,206 g = 206 mg
(en respectant le nombre de chiffres significatifs , on devrait indiquer 2,1.10-4 kg
2) Pour le lot de 80 kg, il faut donc une quantité de cuivre d'environ :
mtotal = 18 000 m = 18 0000 x 2,06.10-4 = 3,71 kg ; ( il y a 18 000 rondelles ŕ cuivrer)
3) La quantité d'électricité qui doit circuler pour réaliser ce dépôt est de :
D'aprčs la demi-équation, n(e-) = 2 n(Cu)formé = 2 m(Cu) / M(Cu) = 2 x 3,71.103 / 63,5 = 117 mol
Q = n(e-) . F = 117 x 96500 = 1,13.107 C
4) L’intensité du courant est constante et égale ŕ 1200 A. La durée de l'opération est donc d'environ :
Q = I . t Ţ t = Q / I = 1,13.107 / 1200 = 9,42.103 s = 157 min
©Sciences Mont Blanc
Correction Bac Réunion Juin 2004 - III ) La catalyse homogène :
I ) Etude cinétique de la transformation chimique
1) Tableau descriptif de l'évolution du systčme chimique
a)
|
Equation chimique |
5 H2O2(aq) + C4H4O62-(aq) + 2 H3O+(aq) = 10 H2O(l) + 4 CO2 (g) |
|||||
|
Avancement (mol) |
Quantités de matičre (en mol) |
|||||
|
Etat initial |
0 |
n1 |
n2 |
excčs |
excčs |
0 |
|
Etat intermédiaire |
x |
n1 - 5x |
n2 - x |
excčs |
excčs |
4 x |
|
Etat final |
xmax = n1/5 |
0 |
n2 - n1/5 |
excčs |
excčs |
4 n1/5 |
n1 < 5 n2. L'eau oxygénée est donc en défaut par rapport aux ions tartrate.
Les erreurs sont corrigées en rouge dans ce tableau.
b) Le milieu doit ętre légčrement acidifié car la réaction a besoin d'ions oxonium H3O+ .
c)
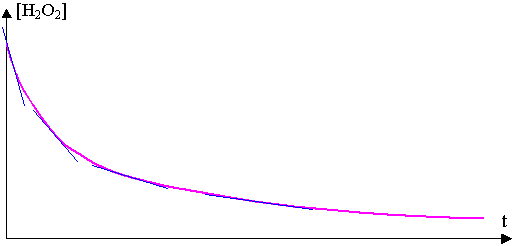
L'eau oxygénée est un réactif, il est donc consommé au cours du temps, sa concentration diminue.
La tangente ŕ la courbe a un coefficient directeur qui diminue au cours du temps, cela correspond ŕ la vitesse volumique de réaction qui diminue car la concentration des réactifs diminue.
2) Etude de la vitesse volumique de réaction
a) v = (1/V).dx/dt avec V = V1+V2 volume totale de la solution.
b) [H2O2] = n(H2O2) / V = (c1.V1 – 5 x ) / V ; (1/V).d[H2O2]/dt = - 5.(1/V).dx/dt
v = - (1/5).d[H2O2]/dt
c) La vitesse diminue au cours du temps. La tangente ŕ la courbe a un coefficient directeur qui diminue au cours du temps, cela correspond ŕ la vitesse volumique de réaction qui diminue car la concentration des réactifs diminue au cours du temps. C'est un facteur cinétique.
II ) Catalyse homogčne :
1) Etude de la courbe 1
a) La méthode physique la plus adaptée pour le suivi temporel de la concentration en ions cobalt III Co3+(aq) présents dans le mélange réactionnel est la colorimétrie car les ions Co3+ sont roses .
En mesurant l'absorbance A de la solution, on peut calculer la concentration en ions Co3+ , proportionnelle ŕ A.
b) Dans les zones 2 et 4, le mélange réactionnel a une couleur verdâtre.
La couleur du mélange réactionnel dans les zones 1 et 5, est rose car les ions Co2+ sont en quantité importante. Dans la zone 3, la couleur du mélange réactionnel est verte car ce sont les ions Co3+ qui imposent leur couleur ŕ la solution.
c) Parmi les réactions chimiques proposées (R1 et R2) quelle est celle qui a lieu dans la zone 2 ? Dans la zone 3 ? Dans la zone 4 ? Justifier vos choix.
2) Vitesse de réaction
Pour déterminer la vitesse volumique de réaction, v, ŕ un instant t3 ŕ partir de la courbe 1, on trace la tangente ŕ la courbe ŕ cet instant et on calcule son coefficient directeur a.
Cette valeur correspond ŕ la valeur de d[Co3+]/dt ŕ l'instant t3. On a alors : v = - a/10.
Il faut tenir des différentes unités , convertir le temps en seconde et la concentration en mol.L-1 .
3) Rôle du catalyseur
a) La courbe 1 met en évidence cette propriété car on constate que les ions Co3+ sont formés puis consommés , les ions Co2+ sont régénérés en fin de réaction, tout ce passe comme s'ils étaient des ions spectateurs sans intervenir.
b) La quantité de matičre finale de dioxyde de carbone obtenu est-elle inchangée avec la présence du catalyseur. Un catalyseur ne modifie pas la réaction sur le plan quantitatif, il permet de l'accélérer.
c) La catalyse est homogčne car le catalyseur et les réactifs sont dans la męme phase.
©Sciences Mont Blanc
Correction Bac Réunion Juin 2004 - I ) (spécialité) Détermination du degré alcoolique d'un vin :
I ) Extraction de l'éthanol :
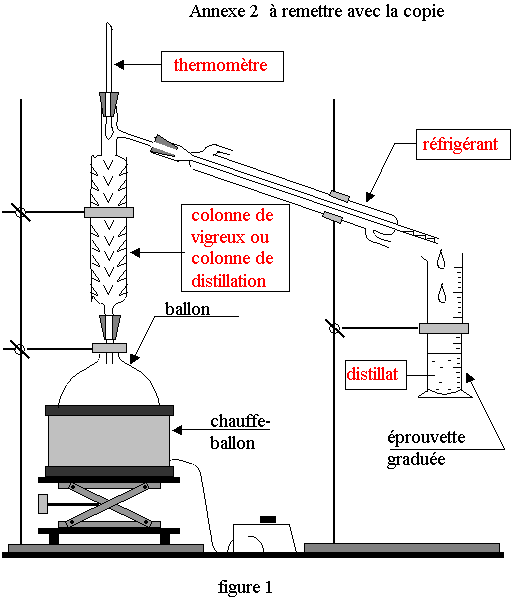
1) Voir figure 1 de l'annexe 2.
III ) Réaction entre l'éthanol et le dichromate de potassium
1) La couleur de la solution S3 est due aux ions Cr3+ verts.
2) On bouche l'erlenmeyer pour éviter le contact du dioxygčne de l'air.
3) 2 Cr2O72– + 16 H3O+ + 3 CH3–CH2OH = 4 Cr3++ 27 H2O + 3 CH3–COOH
D'aprčs l'équation, on a : 3 n(Cr2O72-)consommé = 2 n(éthanol)consommé = 2 n0
n(Cr2O72-) restant = n(Cr2O72-) initial - n(Cr2O72-) consommé = C1.V1 – 2/3 n0
IV ) Dosage de l'excčs du dichromate de potassium :
Cr2O72– + 14 H3O+ + 6 Fe2+ = 2 Cr3++ 21 H2O + 6 Fe3 +
1) D'aprčs l'équation, on a : 6 n(Cr2O72-)consommé = n(Fe2+ )consommé = C2.V2
n(Cr2O72-)consommé = C1.V1 – 2/3 n0 = C2.V2/ 6
n0 = (3/2) (C1.V1 – C2.V2/ 6 ) = 3/2 C1.V1 – 1/4 C2.V2.
2) n0 = 3/2 x 1,00.10-1 x 20,0.10-3 – 1/4 x 5,00.10-1 x 7,6.10-3 = 2,05.10-3 mol
V ) Exploitation :
1) n0 est la quantité d'éthanol dans 10 mL de solution S2.
S2 contient l'éthanol présent dans les 10 mL de vin prélevé, dilué 10 fois.
néthanol (100 mL) = ( 10 n0 / V0) x 100 = 10 x 2,05.10-3 x 100/10,0 = 2,05.10-1 mol
2) degré alcoolique du vin : d° = Véthanol / Vvin = (néthanol.Méthanol/réthanol) / Vvin
d° = (2,05.10-1 x 46 / 0,78) / 100 = 0,12 = 12 %
3) a) La correction ŕ apporter ŕ la valeur d = 12° inscrite sur l'étiquette est de – 0,19, soit 11,8%
b) Le résultat du dosage est en accord avec la valeur corrigée de ce degré en tenant compte de la précision du résultat.
©Sciences Mont Blanc
