Sujet Bac Antilles Septembre 2005
Calculatrice autorisée
I ) Une équation au service des Sciences Physiques ( 9,5 points)
II ) A quoi est due la couleur des fleurs d'hortensias ? ( 2,5 points)
III ) La menthe poivrée ( 4 points)
III ) Séparation des éléments fer et cuivre (spe) ( 4 points)
Antilles Septembre 2005 - I ) Une équation au service
des Sciences Physiques :
L'équation différentielle dx/dt + a.x = b (1) (1), ( a et b étant
des grandeurs constantes), permet de décrire un grand nombre de phénomènes
physiques variables au cours du temps: intensité, tension, vitesse, grandeur
radioactive.
On rappelle que mathématiquement cette équation admet en particulier 2 solutions :
x(t) = (b / a).(1 – e- a . t ) si b ¹ 0 (2) et x(t) = x0 . e - a . t si b = 0 avec x0 grandeur constante
Partie A : Dans le domaine des systèmes électriques :
Cette première partie tend à montrer la validité du modèle pour un circuit électrique mettant en jeu une bobine d'inductance L et de résistance r = 11,8 W ,(donc non négligeable), et un conducteur ohmique de résistance R = 12 W, alimenté par un générateur délivrant une tension continue E = 6,1 V.
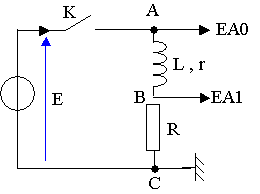
On réalise expérimentalement le circuit électrique ci-contre. L'évolution des grandeurs variables, tension u(t) et intensité i(t), est obtenue par voie informatique.
· La voie EA0 permet de visualiser la tension E
· La voie EAl permet de visualiser la tension UBc
Etude expérimentale
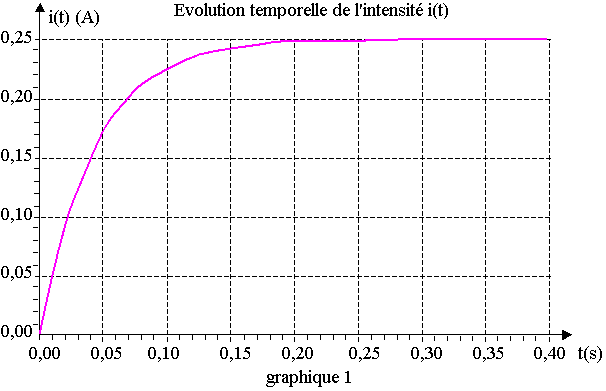
La courbe expérimentale donnant l'évolution de l'intensité i(t), obtenue par traitement informatique est donnée en Annexe n°1, graphique 1 .
Evaluer graphiquement la durée du régime transitoire. Aucune justification n'est demandée.
t étant la constante de temps associée au dipôle {bobine-conducteur ohmique} :
Donner l'expression littérale de t en fonction des paramètres du circuit.
En déduire l'expression de l'inductance de la bobine et calculer sa valeur (elle doit être comprise entre 0,95 H et 1,20 H).
Modèle théorique
En utilisant la loi d'additivité des tensions et en respectant l'orientation du circuit, établir l'équation différentielle vérifiée par l'intensité i(t).
Par identification avec l'équation (1) vérifier que a = ( R + r ) / L et donner l'expression de b.
En déduire l'équation horaire littérale i(t) en fonction de {r, R, L et E}. Montrer que cette solution valide bien l'équation établie en 2.1.
Montrer que cette équation horaire peut s'écrire i(t) = E.( 1 – e – t / t ) / (R + r) .
Confrontation des résultats expérimentaux avec le modèle théorique.
On rappelle que lim x ® - ¥ ( e x ) = 0 et e 0 = 1
On appellera I l'intensité en régime permanent (l'intensité étant constante).
Donner l'expression littérale de I. Calculer sa valeur.
Est-elle en accord avec la valeur expérimentale obtenue ?
Donner l'expression littérale de i(t) à la date t = t en fonction de I. Calculer sa valeur. Est-elle en accord avec l'expérience ?
Partie B : Dans le domaine mécanique :
L'étude de la chute d'une bille d'acier, de masse m, dans un fluide de masse volumique rfluide a été exploitée grâce à un logiciel.
Les capacités du logiciel permettent ensuite de faire tracer l'évolution de la vitesse du centre d'inertie en fonction du temps.
Les deux courbes, expérimentale et modélisée, sont proposées ci-dessous, mais ne donnent lieu à aucune exploitation.
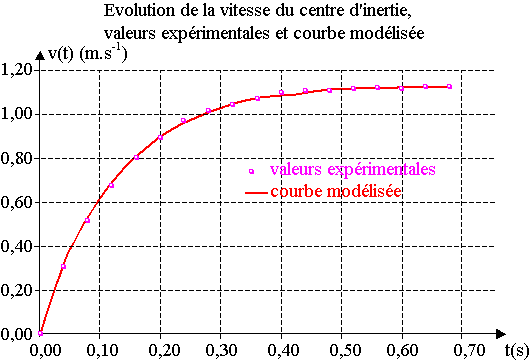
Exploitation de l'équation v(t) modélisée.
L'équation mathématique associée à la courbe modélisée, vérifie v(t) = 1,14 ( 1 – e – t / 0,132 ) (3) , avec v(t) en m.s-1 et t en s. Cette équation est identifiable à l'équation (2).
Déterminer la valeur de a et du rapport b / a . Donner, sans justification, l'unité du rapport b / a .
Montrer que l'équation
différentielle ayant l'équation (3) pour solution vérifie l'écriture
numérique dv/dt + 7,58 v = 8,64 .
Etude du phénomène physique.
Faire l'inventaire des forces appliquées à la bille. Les représenter sur un schéma, en sens et direction appliquée au centre d'inertie G de la bille.
Appliquer au système bille la seconde loi de Newton.
Exploitation de la modélisation
La bille ayant servi à réaliser l'étude est une bille d'acier de masse m = 32 g et de volume V.
L'accélération de la pesanteur est g = 9,81 m.s-2.
Les forces de frottement qui s'appliquent à la bille ont pour expression f = - k. v .
En utilisant un axe vertical orienté vers le bas, montrer que l'équation différentielle relative à la grandeur variable v(t) vérifie
dv/dt + (k / m) . v = ( 1 – rfluide . V / m ).g .
En déduire l'expression littérale des coefficients a et b de l'équation (1).
Quelle serait la valeur du coefficient b si la poussée d'Archimède était nulle ? En utilisant l'équation établie en 1.2., justifier que cette force doit être prise en compte.
Partie C : Dans le domaine de la radioactivité :
Les traceurs radioactifs sont des radio-isotopes très utilisés en imagerie médicale pour l'exploration des organes.
Des dispositifs adaptés transforment en image les mesures d'activité enregistrées.
Le 11C est un traceur radioactif utilisé pour suivre en particulier l'évolution de la maladie de Parkinson.
Le traceur radioactif se fixe sur le cerveau. L'activité moyenne résiduelle évolue au cours du temps selon la loi
A(t) = A0.e - l . t (4).
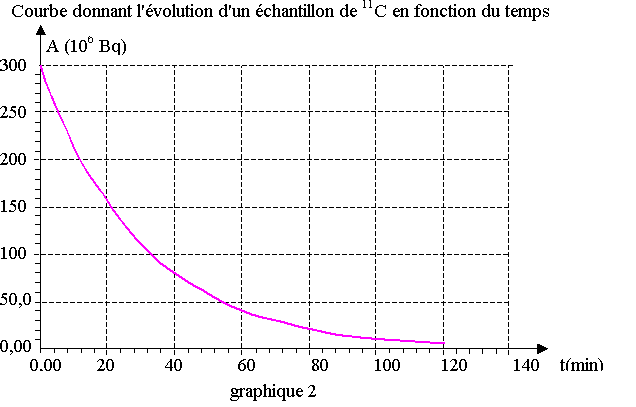
L'évolution de l'activité d'un échantillon de 11C est donnée sur le graphique 2 de l'Annexe n°1.
On va utiliser ce graphique pour atteindre les grandeurs radioactives caractéristiques du 11C.
Montrer par analyse dimensionnelle que l (constante radioactive), est identifiable à l'inverse d'un temps.
Rappeler la relation liant l à la constante de temps t du radio isotope.
Exprimer la loi d'évolution A(t) en fonction de t.
Evaluer graphiquement la valeur de la constante de temps t et en déduire la valeur de l.
On prendra par la suite l = 3,40.10–2 min-l.
Définir le temps de demi-vie t½ , le déterminer graphiquement.
A(t) = A0. e - l . t étant solution de l'équation différentielle dA/dt + l . A(t) = 0, on se propose d'utiliser la méthode itérative d'Euler pour résoudre cette équation.
On rappelle que pour une grandeur variable x(t), la méthode d'Euler permet d'écrire :
x(t + Dt) = x(t) + (dx/dt).Dt
Exploiter cette équation pour établir la relation liant A(t+Dt), A(t), l et Dt.
L'activité initiale de la dose injectée au patient est A0 = A(t0) = 3,00.108 Bq.
La méthode d'Euler impose de se fixer un pas Dt pour effectuer les calculs.
Justifier que la valeur Dt = 15 min n'est pas correctement adaptée à l'étude.
On choisit de faire les calculs avec un pas Dt = 5 min. Recopier et compléter le tableau ci-dessous mettant en parallèle les résultats obtenus avec la méthode d'Euler et ceux obtenus à partir de l'équation théorique (4).
|
Date (min) |
A Euler (Bq) |
A théorique (Bq) |
|
0 |
3,00.108 |
3,00.108 |
|
5 |
2,53. 108 |
|
|
10 |
2,07.108 |
|
|
15 |
1,72.108 |
1,80.108 |
On considérera que le choix de Dt est pertinent si l'écart relatif entre A Euler et A théorique est inférieur à 5%. La valeur proposée pour Dt vous semble-t-elle correctement adaptée ?
Annexe n°1 à rendre avec la copie
©Sciences Mont Blanc
Antilles Septembre 2005 - II ) A quoi est due
la couleur des fleurs d'hortensias :
Certaines fleurs, comme celles des hortensias, possèdent des couleurs variées dues à des pigments naturels.
Les couleurs rouge, mauve, violette et bleue viennent de la présence d'anthocyanines dans les pétales.
La couleur violette est due à la molécule suivante que l'on notera HA dans la suite de l'exercice.
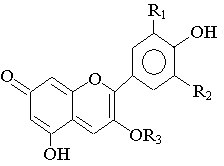

1 ) Introduction
HA peut appartenir à deux couples H2A+ / HA de pKa1 = 4,3 et HA / A– de pKa2 = 7
L'espèce H2A+ est rouge, l'espèce HA est violette et l'espèce A– est bleue.
On rappelle que pKe = 14.
Donner la définition d'un acide selon Brönsted.
Préciser dans chacun des 2 couples la forme acide et la forme basique.
2 ) Comportement de HA en tant qu'acide.
2.1) Ecrire l'équation de la réaction de HA en tant qu'acide avec l'eau.
2.2) Donner l'expression de la constante d'équilibre de cette réaction.
Comment appelle-t-on cette constante ? Donner sa valeur.
Le pH d'une solution contenant HA est de 10.
2.3) A partir de l'expression de K, évaluer littéralement, puis calculer le rapport [A-]éq / [HA]éq
2.4) En déduire l'espèce prédominante. Conclure sur la couleur de la solution.
3 ) Comportement de HA en tant que base.
3.1) Ecrire l'équation de la réaction de HA en tant que base avec l'eau.
3.2) Donner l'expression de la constante d'équilibre K ' de cette réaction.
Quelle est la relation entre Ka1 et K ' ?
4 ) Conclusion : Couleur des hortensias.
4.1) Placer sur un diagramme les domaines de prédominance des espèces H2A+ , HA et A– suivant les valeurs du pH.
4.2) Pourquoi les fleurs d'hortensias peuvent-elles changer de couleur suivant la nature du sol ?
©Sciences Mont Blanc
Antilles Septembre 2005 - III ) La menthe poivrée :

La menthe poivrée, calmante (maux de tête, coups de soleil) mais aussi stimulante, digestive, antispasmodique et antiseptique est bien connue pour ses bienfaits depuis des siècles.
Utilisée en parfumerie, son huile essentielle contient un ester très odorant: l'éthanoate de menthyle que l'on peut synthétiser en laboratoire, à partir de menthol et d'un acide carboxylique.
1 ) Préliminaires :
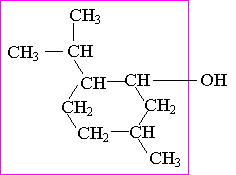 Le
menthol a pour formule semi-développée :
Le
menthol a pour formule semi-développée :
Dans la suite de l'exercice, on le notera pour simplifier R–OH
R est le groupement encadré ci-contre.
1.1) A quelle famille chimique appartient le menthol ?
1.2) Donner le nom et la formule semi-développée de l'acide carboxylique qui, par réaction avec le menthol, permet de synthétiser l'éthanoate de menthyle.
1.3) A l'aide des formules semi-développées (simplifiée pour le menthol), écrire l'équation de la réaction de synthèse de l'ester.
1.4) On mélange à l'instant initial 0,10 mol d'acide carboxylique précédent et 0,10 mol de menthol. Donner l'expression du quotient de réaction Qr et calculer sa valeur à l'instant initial.
1.5) La constante d'équilibre K associée à cette réaction est égale à 2,3 à 70°C.
Quel est le sens d'évolution spontanée du système ?
2 ) Synthèse de l'éthanoate de menthyle.
Protocole expérimental de l'expérience n°1:
Afin de synthétiser l'éthanoate de menthyle, on introduit dans un erlenmeyer maintenu dans la glace :
0,10 mol d'acide carboxylique précédent
0,10 mol de menthol
quelques gouttes d'acide sulfurique concentré
On répartit de façon égale le mélange dans 10 tubes à essais que l'on surmonte d'un réfrigérant à air. On plonge simultanément les 10 tubes dans un bain marie thermostaté à 70°C et on déclenche le chronomètre.
A intervalles de temps réguliers, on place un tube à essai dans un bain d'eau glacée et on dose l'acide restant par une solution d'hydroxyde de sodium (Na +(aq) + HO -(aq)) en présence d'un indicateur coloré approprié.
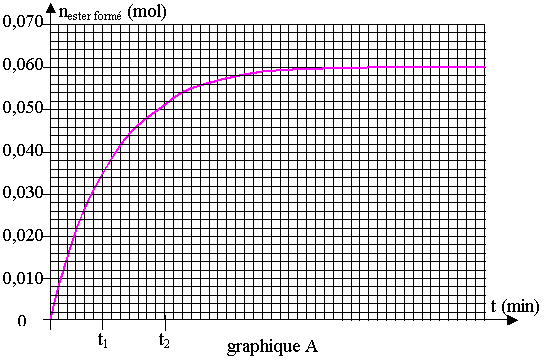
Les résultats obtenus permettent de tracer la courbe d'évolution de la quantité de matière d'ester formée en fonction du temps
( nester formé = f ( t )) donnée en Annexe graphique A :
Pourquoi faut-il placer les tubes à essais dans la glace avant titrage ? Justifier votre réponse.
Ecrire, à l'aide des formules semi-développées, l'équation de la réaction associée au titrage de l'acide carboxylique par la solution d'hydroxyde de sodium.
3 ) Exploitation des résultats :
Compléter le tableau d'avancement associé à la réaction écrite en 1.3 proposé en Annexe et à rendre avec la copie et déterminer xmax.
A l'aide de la courbe précédente, calculer le rendement de la réaction. Conclure.
Exprimer le quotient de réaction à l'équilibre en fonction de l'avancement final xf et des quantités de matière initiales.
A l'aide de la valeur de xf expérimental déterminer la valeur de la constante d'équilibre K.
Est-elle cohérente avec celle fournie dans la partie 1 ?
Comment évaluer graphiquement la vitesse de la réaction ?
Comparer les vitesses v1 (à t = t1) et v2 (à t = t2 ) et justifier l'évolution de la valeur de la vitesse de la réaction au cours du temps.
4 ) Influence des conditions expérimentales :
On réalise 3 autres expériences de façon analogue à l'expérience n°1 mais en faisant varier les conditions expérimentales (température, quantité de matière initiale des réactifs) suivant le tableau ci-dessous :
|
Quantité de matière (en mol) |
Expérience n°1 |
Expérience n°2 |
Expérience n°3 |
|
Acide carboxylique |
0,10 |
0,10 |
0,20 |
|
Menthol |
0,10 |
0,10 |
0,10 |
|
Température ( °C) |
70 |
20 |
70 |
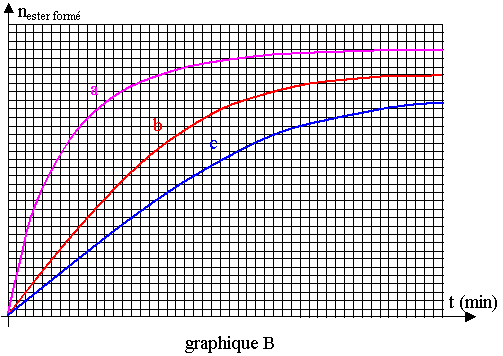
On trace à nouveau les courbes nester formé = f(t) et on obtient les allures données en Annexe graphique B :
Attribuer, en justifiant votre réponse, les courbes a, b et c aux conditions expérimentales 1, 2 et 3.
Annexe à rendre avec la copie
|
Equation |
………… + ROH = ………… |
||||
|
Etat |
Avancement |
Quantités de matière |
|||
|
Initial |
0 |
||||
|
Intermédiaire |
x |
||||
|
Final |
xf |
||||
©Sciences Mont Blanc
Antilles Septembre 2005 - III ) Séparation des éléments
fer et cuivre (spe) :
Le minerai de cuivre contient des impuretés en particulier du fer. A partir de ce minerai, on prépare une solution aqueuse contenant des ions cuivre II (Cu2+(aq)) et des ions fer III (Fe3+(aq)).
Le but de l'exercice est de comparer deux méthodes possibles
pour réaliser la séparation des ions Cu2+(aq) des ions
Fe3+(aq) présents dans une même solution. Cette séparation
ne nécessite pas que les éléments fer et cuivre soient en solution aqueuse
à la fin des transformations envisagées.
Données : La constante de réaction Ke associée à la réaction d'autoprotolyse de l'eau
2H2O(l) = H3O+(aq) + HO–(aq) est Ke = 10–14 (à 25°C)
Masses molaires atomiques : M(Fe) = 55,8 g.mol–1 ; M(Cu) = 63,5 g.mol–1.
1 ) Première partie : Une technique par précipitation :
1.1) Etude portant sur les ions Cu2+(aq).
L'ajout d'une solution d'hydroxyde de sodium (Na+(aq) + HO–(aq)) dans une solution contenant des ions Cu2+(aq) donne naissance à un précipité bleu d'hydroxyde de cuivre Cu(HO)2 (s).
Cette transformation est modélisée par :
Cu2+ (aq) + 2 HO– (aq) = Cu(HO)2 (s)
La constante de réaction K1 associée à cette transformation est K1 = 4,0.1018.
La formation du précipité dépend du pH de la solution.
On réalise l'expérience suivante :
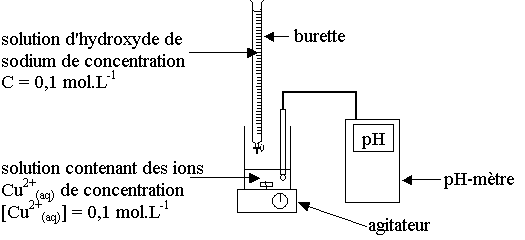
Les résultats sont exploités à l'aide d'un logiciel qui permet de tracer les courbes représentant les pourcentages respectifs des espèces Cu2+ (aq) et Cu(HO)2 (s) présentes dans la solution en fonction du pH.
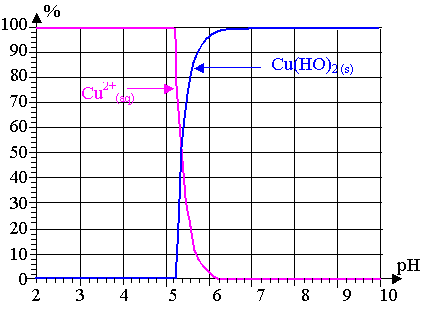
1.1.1) A l'aide de ces courbes, donner la valeur du pH pour laquelle le précipité Cu(HO)2 (s) apparaît.
1.1.2) Sens d'évolution de la réaction.
1.1.2.1) Donner l'expression de K1.
1.2.2.2) Pour un volume de solution d'hydroxyde de sodium ajouté, on peut définir le quotient de réaction noté Qr. Exprimer Qr.
1.2.2.3) Dans quel sens évolue la réaction si Qr < K1 ?
1.1.3) On étudie maintenant l'apparition du précipité. On a alors Qr = K1 et la concentration en ions Cu2+ (aq) à l'équilibre, notée [Cu2+(aq)]éq, vaut toujours 0,10 mol.L–1 . Montrer que la valeur de la concentration en ions hydroxyde notée [HO–(aq)]éq vaut 1,6.10–9 mol.L-1 .
1.1.4) En déduire la valeur du pH de la solution. Conclure.
1.2) Etude portant sur les ions Fe3+ (aq)
On réalise la même expérience en remplaçant la solution contenant des ions Cu2+ (aq) par une solution contenant des ions Fe3+ (aq) à la même concentration de 0,1 mol.L–1.
La transformation chimique qui se déroule peut être décrite par la réaction :
Fe3+ (aq) + 3 HO– (aq) = Fe(HO)3 (s)
Fe(HO)3 (s) est un précipité de couleur rouille.
La courbe donnant les pourcentages respectifs des espèces
Fe3+ (aq) et Fe(HO)3 (s) présentes dans la
solution en fonction du pH de cette dernière est la suivante :
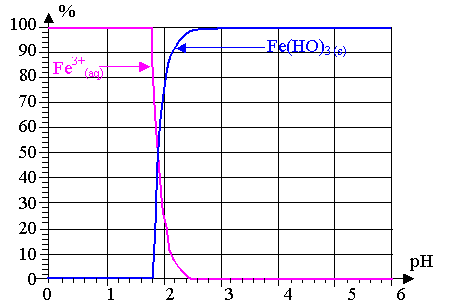
1.2.1) La solution contient-elle des ions Fe3+ en quantité significative pour un pH supérieur à 3,5 ?
1.2.2) On reprend le montage de la question 1.1. en plaçant dans le becher une solution constituée de :
- 10 mL de solution de chlorure de fer (III) (Fe3+ (aq) + 3 Cl– (aq))
- 10 mL de solution de sulfate de cuivre (II) (Cu2+ (aq) + SO42– (aq))
Dans cette solution: [Cu2+ (aq)] = [Fe3+ (aq)] = 0,1 mol.L–1 .
Le pH du mélange initial est faible. Un élève désirant séparer les ions Cu2+ (aq) des ions Fe3+ (aq) ajoute alors la solution d'hydroxyde de sodium pour que le pH du mélange atteigne la valeur 4,0. Il filtre ensuite le mélange obtenu dans le becher, la solution obtenue est appelée S1.
1.2.2.1) Sous quelle forme est obtenue l'espèce extraite de la solution ?
1.2.2.2) Quelle est l'espèce chimique présente dans la solution S1 ?
1.2.2.3) Comment vérifier que la solution S1 ne contient plus qu'une seule des espèces chimiques Cu2+ (aq) ou Fe3+ (aq) présentes initialement ?
2 ) Deuxième partie : Technique par oxydo-réduction :
Les ions cuivre (II) Cu2+(aq) réagissent avec le métal fer pour donner naissance au cuivre métal et aux ions fer (II) Fe2+(aq) . La transformation peut être décrite par la réaction d'équation :
Cu2+(aq) + Fe (s) = Cu (s) + Fe2+(aq) (réaction 3)
Les ions fer (III) réagissent avec le métal fer pour donner des ions fer (II) Fe2+ (aq).
La transformation peut être décrite par la réaction d'équation :
2 Fe3+(aq) + Fe (s) = 3 Fe2+(aq) (réaction 4)
On dispose d'une solution S1 de volume V1 = 200 mL contenant des ions Cu2+ (aq) et Fe3+ (aq).
Dans un becher contenant la totalité de cette solution, on ajoute 10 g de fer en poudre, on estimera que cette masse est suffisante pour que la totalité des ions cuivre (II) et fer (III) réagisse.
2.1) On considère que les réactions (3) et (4) sont totales.
Sous quelle forme l'élément cuivre initialement présent dans la solution S1 se retrouve-t-il à la fin de la réaction ?
2.2) Sous quelle forme l'élément fer initialement présent dans la solution S1 se retrouve-t-il à la fin de la réaction.
2.3) A-t-on réalisé la séparation désirée ?
3 ) Conclusion :
On dispose d'une solution contenant des ions Cu2+(aq) et des ions Fe3+(aq) , ces derniers étant présents en très faible quantité. Cette solution doit être utilisée pour préparer du cuivre métallique par électrolyse des ions Cu2+(aq), il est donc nécessaire d'éliminer les ions Fe3+(aq).
Quelle méthode (précipitation ou oxydo-réduction) doit-on utiliser ?
©Sciences Mont Blanc