Correction Bac Liban - Juin 2008![]()
Calculatrice autorisée
I ) Découverte d'une exo-planète habitable (5,5 points)
II ) Détermination expérimentale du pKa d'un indicateur coloré : Le bleu de bromophénol (6,5 points)
III ) 1932 : Le radium à la mode ... (4 points)
III ) Etude d'un piano (4 points) (spe)
Correction Bac Liban - Juin 2008 - I ) Découverte d'une exo-planète habitable :
Premičre partie
 1.1) schéma
1.1) schéma
1.2) F = G . MC . m / (RC+h)2
1.3) g = F / m . A la surface de C , h = 0 m ; g0 = F / m = G . MC / RC2
2.1) On applique la 2čme loi de Newton dans le référentiel galiléen lié au centre de la plančte C en utilisant le repére de Frenet :
 = m .
= m . 
 =
=  N +
N +  T = v2 /(RC+h) .
T = v2 /(RC+h) . 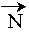 +
dv/dt .
+
dv/dt .  ;
;
 = F .
= F . 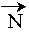
m . ( v2 /(RC+h) . 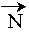 + dv/dt .
+ dv/dt .  ) = F .
) = F . 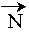 ; m
. v2 / (RC+h) = F
et dv/dt = 0
; m
. v2 / (RC+h) = F
et dv/dt = 0
m . v12 / (RC+h) =
G . MC . m / (RC+h)2 ; v12
= G . MC / (RC+h) ; v1 =  (G . MC / (RC+h) )
(G . MC / (RC+h) )
2.2) Si h est négligeable
devant RC , v1
=  (G . MC / RC
)
(G . MC / RC
)
3) V2
=  (2 G . M / R)
; si R augmente V2
diminue.
(2 G . M / R)
; si R augmente V2
diminue.
4.1) g0 = G . MC / RC2 ; G
. MC / RC = g0 . RC ; V2 =  (2 g0 . RC)
(2 g0 . RC)
4.2) V2
=  ( 2 x 22 x 9,6.106)
= 2,1.104 m.s-1 = 21 km.s-1
( 2 x 22 x 9,6.106)
= 2,1.104 m.s-1 = 21 km.s-1
V2 est supérieure ŕ la vitesse de libération de la Terre.
4.3) L'existence d'une atmosphčre est compromise si V2 est faible or celle de la plančte C est supérieure ŕ celle de la Terre, l'existence d'une atmosphčre sur la plančte C est donc possible.
Deuxičme partie :
1) M est ici la masse de l'étoile E.
2.1) Dans le référentiel de l'étoile E, le rapport entre le carré de la période de révolution T d’une plančte autour de l'étoile et le cube du rayon r est constant :
T2 / r3 = constante
2.2) Tc2 / rc3 = (12,93)2 / (7,27.10-2)3 = 4,35.105 USI ; Td2 / rd3 = (84,4)2 / (2,54.10-1)3 = 4,35.105 USI
2.3) Tb2 / rb3
= k ;
rb = 3  (Tb2 / k) = 3
(Tb2 / k) = 3  (5,3662 / 4,35.105) = 4,05.10-2 U.A.
(5,3662 / 4,35.105) = 4,05.10-2 U.A.
Troisičme partie :
1) "L'énergie des molécules est quantifiée" signifie que les niveaux d'énergie des molécules ont une valeur définie et distincte. Les transitions possibles entre ces niveaux d'énergie sont donc définis.
2) Le domaine de longueur d'onde du visible est compris entre 400 et 800 nm. 1 μm = 1000 nm
Ces radiations ont une longueur d'onde supérieure ŕ celles du domaine visible, ce sont des radiations infra-rouges .
3) ΔE = E1 – E0 = h . ν = h . c / λ
λ = h . c / (E1 – E0) = 6,626.10-34 x 3,00.108 / (0,20 x 1,6.10-19) = 6,2.10-6 m = 6,2 μm
©Sciences Mont Blanc
Correction Bac Liban - Juin 2008 - II ) Détermination expérimentale du pKa d'un indicateur coloré : Le bleu de bromophénol :
Premičre partie
1) n0 = C0 . V = 3,0.10-5 x 0,100 = 3,0.10-6 mol
2.1) Un acide selon Bronsted est une espčce chimique capable de céder un proton H+ .
2.2) couples : HIn / In- et H3O+ / H2O
3.1)
|
Equation chimique |
HIn(aq) + H2O(l) = In-(aq) + H3O+(aq) |
||||
|
Etat du systčme |
Avancement |
Quantité de matičre en mol |
|||
|
Etat initial |
x = 0 |
n0 |
excčs |
0 |
0 |
|
Etat intermédiaire |
x |
n0 - x |
excčs |
x |
x |
|
Etat final si réaction totale |
x = xmax |
n0 - xmax |
excčs |
xmax |
xmax |
|
Etat final observé |
x = xf |
n0 - xf |
excčs |
xf |
xf |
3.2) L'eau est en excčs, HIn est en défaut : n0 – xmax = 0 ; xmax = n0 = 3,0.10-6 mol.
3.3) xf = n(H3O+)f = [H3O+] . V = 10-pH . V = 10-4,7 x 0,100 = 2,0.10-6 mol
3.4) τ = xf / xmax = 2,0.10-6 / 3,0.10-6 = 0,67 = 67 % ; τ < 1 , la réaction n'est pas totale, elle est limitée.
4.1) n(HIn) = n0 – x ; n(In-) = x ; n(HIn) = n0 – n(In-) ; n(HIn) + n(In-) = n0
4.2) On divise la relation précédente par V : [HIn] + [In-] = C0
Deuxičme partie
1) Dans la solution S1 acide, HIn espčce jaune prédomine. Dans la solution S2 basique, In- espčce bleue prédomine.
2) La proportion d'acide et de base conjuguée dépend de la concentration d'ions oxonium H3O+ , du pH de la solution.
3) Si [HIn] est négligeable, [In-] est égale ŕ C0 .
Troisičme partie
1.1) D'aprčs l'énoncé, ŕ la longueur d'onde λ utilisée par le spectrophotomčtre, seule la forme basique In- absorbe, on a donc : A = k . [In-].
1.2) Au pH de 12,0, la solution est trčs basique, HIn est négligeable devant In-, [In-] = C0 .
A = Amax = k . [In-] = k . C0 . k = Amax / C0 = 1,66 / 3,0.10-5 = 5,5.104 L.mol-1
1.3) [In-] = A / k = 0,83 / 5,5.104 = 1,5.10-5 mol.L-1
[Hin] = C0 – [In-] = 3,0.10-5 – 1,5.10-5 = 1,5.10-5 mol.L-1 = [In-]
 2.1) voir graphique
2.1) voir graphique
2.2) Ka = [H3O+] . [In-] / [HIn] ; - log Ka = - log[H3O+]+log([HIn]/[In-])
pKa = pH + log([HIn] / [In-]) ; pH = pKa + log([In-] / [HIn])
2.3) Lorsque [Hin] = [In-], log([In-] / [HIn]) = 0 , pH = pKa.
D'aprčs le graphique, les 2 courbes se croisent ŕ pH = pKa = 3,9.
2.4) La solution S2 a un pH de 12,0. [H3O+ ] = 1,0.10-12 mol.L-1
[In-] / [HIn] = Ka / [H3O+] = 10-3,9 / 1,0.10-12 = 1,3.108 >> 104
HIn est donc bien négligeable devant In- .
©Sciences Mont Blanc
Correction Bac Liban - Juin 2008 - III ) 1932 : Le radium à la mode ... :
Premičre partie
1.1) Le noyau de radium est composé de 88 protons ( Z = 88) et de 138 neutrons (226 – 88).
1.2) Lois de Soddy : Lors d'une désintégration nucléaire, il y a conservation du nombre de charge Z et du nombre de nucléons A.
La particule α est 42He. Le noyau fils a donc 86 protons (88 – 2) et 222 neutrons (226 – 4).
22688Ra → 22286Rn + 42He
2.1) m(226Ra) = n . M = (N0 / NA) . M = ( 3,33.1014 / 6,02.1023) . 226 = 1,25.10-7 g
La phrase illustrant ce résultat est "Le Tho-Radia revendique haut et fort sa faible teneur en radium"
2.2.1) Loi de décroissance : N(t) = N0 . e- λ . t
2.2.2) pourcentage de noyaux restants ŕ la date de 10 ans :
N(10ans) / N0 = exp ( - 1,35.10-11 x 10 x 365,25 x 24 x 60 x 60 ) = 0,996 ≈ 100 %
La quantité de radium ne varie presque pas en 10 ans, son activité reste donc la męme.
2.3) t1/2 = ln 2 / λ = ln 2 / 1,35.10-11 = 5,13.1010 s = 1627 jours ≈ 16 sičcles
t ˝ est le temps de demi-vie, temps au bout duquel la moitié des noyaux présents initialement présents ont été désintégrés. Cela correspond bien ŕ la phrase.
 Deuxičme partie :
Deuxičme partie :
1) Sur le graphique, la tangente ŕ l'origine croise l'axe des temps au temps τ.
D'aprčs le graphique, τ vaut 5,5 jours.
2) t1/2 est le temps de demi-vie, temps au bout duquel la moitié des noyaux présents initialement présents ont été désintégrés. A t = t1/2 ,
N(t) = N0 / 2 = N0 . exp( - λ . t1/2 ) ; exp( - λ . t1/2 ) = 1 / 2 ; - λ . t1/2 = ln(1/2)
t1/2
= ln 2 / λ =
τ . ln
2 = 5,5 x ln 2 = 3,8 jours
Cette valeur est en accord avec l'énoncé
3) N0 = N0' / 2 ; τ ne change pas, la tangente ŕ l'origine part de N0 vers τ.
A t1/2, N = N0 / 2 . A 2t1/2, N = N0 / 4
©Sciences Mont Blanc
Correction Bac Liban - Juin 2008 - III ) Etude d'un piano :
©Sciences Mont Blanc


