Sujet Bac Nouvelle Calédonie Mars 2008![]()
Calculatrice autorisée
I ) Stockage de l'énergie solaire" (6,5 points)
II ) Science et sport (5,5 points)
III ) Un conservateur alimentaire (4 points)
Sujet Bac Nouvelle Calédonie Mars 2008 - I ) Stockage de l'énergie solaire" :
" Le Soleil est une étoile quelconque mais, pour la vie sur Terre, sa présence est indispensable…
L’énergie solaire reçue par la Terre représente par an prčs de 15 000 fois la totalité de la consommation énergétique mondiale actuelle ! » (CRDP Nantes)
Une partie de cette énergie abondante peut ętre transformée en énergie électrique par une cellule photovoltaďque (capteur solaire). Cette énergie électrique doit ętre stockée car la demande énergétique peut ętre décalée dans le temps vis-ŕ-vis de l’apport en énergie solaire (utilisation par exemple, d’un éclairage la nuit).
Dans cet exercice, on étudie deux types de stockage de l’énergie électrique fournie par une cellule photovoltaďque :
- le stockage de l’énergie électrique dans un condensateur de grande capacité.
- la production par électrolyse d’un combustible pour une pile électrochimique.
Les deux parties correspondant aux deux types de stockage sont indépendantes.
La charge et la décharge du condensateur peuvent ętre traitées indépendamment.
1) Utilisation d’un condensateur de trčs grande capacité
Le fabriquant du
condensateur utilisé indique une valeur de capacité C = 100 000 µF
![]() 10%.
10%.
1.1) Charge du condensateur ŕ courant constant
Les caractéristiques de la cellule photovoltaďque en régime normal de fonctionnement sont indiquées ci-dessous (toutes les données ne sont pas utiles) :
Puissance : 0,6 W
Intensité : 270 mA
Tension maximale : 2,25 V
Dimensions : 394 ´ 127 ´ 20 mm
Masse : 0,41 kg
Plage de température : - 40 °C ŕ + 60 °C
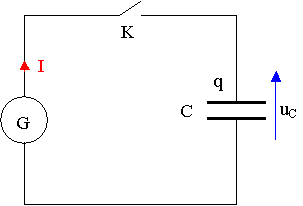 La cellule photovoltaďque se
comporte comme un générateur G débitant un courant d’intensité constante I
= 0,27 A, tant que la tension ŕ ses bornes reste inférieure ŕ la tension maximale
Umax = 2,25 V.
La cellule photovoltaďque se
comporte comme un générateur G débitant un courant d’intensité constante I
= 0,27 A, tant que la tension ŕ ses bornes reste inférieure ŕ la tension maximale
Umax = 2,25 V.
La cellule photovoltaďque est branchée aux bornes du condensateur (figure 1).
A la date t0 = 0 s, on ferme l’interrupteur K et on débute l’enregistrement informatisé des variations de la tension aux bornes du condensateur uC(t) en fonction du temps.
On obtient le graphe de la figure 2, page suivante.
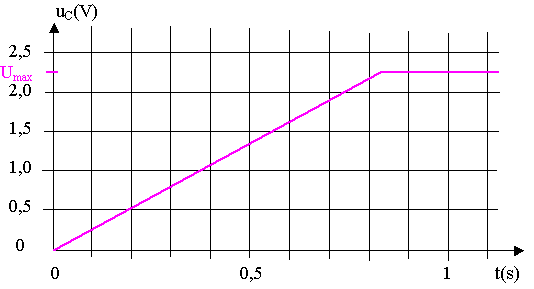
Figure 2 : charge du condensateur
1.1.1) Nommer les deux régimes observables sur le graphe uC = f(t) représenté en figure 2.
1.1.2) Donner l’expression de uC en fonction de C et de la charge q du condensateur.
1.1.3) Le condensateur est initialement déchargé.
Donner l’expression de la charge du condensateur q en fonction de l’intensité I et de la date t lorsque uC est inférieure ŕ Umax (charge ŕ courant constant).
En déduire que uC = I . t / C tant que uC est inférieure ŕ Umax.
1.1.4) Déterminer la valeur et préciser l’unité du coefficient directeur, noté k, de la portion de droite de la figure 2 lorsque uC est inférieure ŕ Umax .
Utiliser ce résultat pour vérifier que la valeur de C est compatible avec les indications du constructeur.
1.1.5) Calculer la quantité d’énergie électrique stockée dans le condensateur lorsque la charge est terminée.
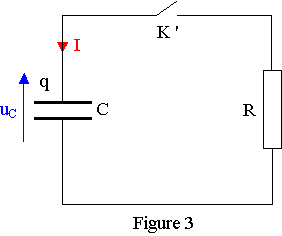 1.2) Décharge du condensateur
dans un conducteur ohmique
1.2) Décharge du condensateur
dans un conducteur ohmique
L’énergie stockée dans le condensateur peut ętre utilisée pour faire fonctionner une lampe (L) de faible puissance que l’on assimile ŕ un conducteur ohmique de résistance R.
On branche en série le condensateur et le conducteur ohmique (figure 3).
A l’instant de date t = 0, le condensateur a une tension ŕ ses bornes égale ŕ Umax et on ferme l’interrupteur K’.
Le graphe donnant uC = f(t) est donné sur la figure 4 de l’annexe.
1.2.1) En respectant les conventions de la figure 3, établir l’expression de i en fonction de uC.
1.2.2) Montrer que l’expression de l’équation différentielle ŕ laquelle satisfait uC lors de la décharge peut s’écrire ; uC + R.C.duC/dt = 0.
1.2.3) Vérifier que uC = Umax . e – t / RC est une solution de l’équation différentielle précédente.
1.2.4) Quel est le signe de i(t) lors de la décharge ? Justifier la réponse.
1.2.5) Déterminer, en faisant apparaître clairement la méthode sur la figure 4 de l’annexe, la valeur de la constante de temps τ du systčme électrique.
Déduire de la valeur de la constante de temps τ la valeur de la résistance R.
1.2.6) On considčre que la lampe (L) fonctionne correctement si la tension imposée par le condensateur entre ses bornes est supérieure ŕ 1,0 V.
On rappelle que l’on assimile la lampe au conducteur ohmique de résistance R.
Déterminer, en utilisant la figure 4 de l’annexe, la durée Δt durant laquelle la lampe fournit une quantité de lumičre suffisante.
Conclure sur l’utilisation de ce condensateur pour un éclairage la nuit.
2) Utilisation d’une pile ŕ combustible
L’énergie électrique fournie par une cellule photovoltaďque permet la production de dihydrogčne gazeux H2(g) par électrolyse de l’eau.
Le dihydrogčne produit est stocké, puis utilisé dans une pile ŕ combustible.
2.1) Electrolyse de l’eau
Afin de réaliser l’électrolyse de l’eau, les bornes de la cellule photovoltaďque sont reliées ŕ deux électrodes de platine immergées dans une solution d’acide sulfurique. Les gaz formés sont récupérés.
L’équation modélisant la transformation ayant lieu lors de l’électrolyse est :
2 H2O(l) = 2H2 (g) + O2 (g)
Les couples oxydant/réducteur mis en jeu sont O2 (g) / H2O(l) et H+(aq) / H2 (g).
2.1.1) L’électrolyse de l’eau est-elle une transformation spontanée ? Justifier.
2.1.2) Ecrire les deux équations d’oxydoréduction correspondant aux transformations ayant lieu aux électrodes.
2.1.3) Quel type de réaction a lieu ŕ l’électrode reliée ŕ la borne négative de la cellule photovoltaďque ? Nommer cette électrode.
2.2) Fonctionnement de la pile
Aprčs douze heures de fonctionnement, l’électrolyseur a produit une quantité de dihydrogčne n(H2) = 6,0´10 –2 mol. Ce dihydrogčne est entičrement utilisé comme combustible dans une pile schématisée sur la figure 5 de l’annexe. La pile consomme, lors de son fonctionnement, du dihydrogčne et du dioxygčne gazeux qui sont introduits au contact d’électrodes poreuses séparées par une solution acide jouant le rôle d’électrolyte. Le seul produit formé est de l’eau.
L’équation modélisant la transformation ayant lieu lors du fonctionnement de la pile est :
2 H2 (g) + O2 (g) = 2 H2O(l).
La valeur d’un faraday est F = 9,65 ´ 104 C.mol –1.
2.2.1) Indiquer sur la figure 5 donnée sur l’annexe les bornes positive et négative du générateur ainsi que la nature et le sens de circulation des porteurs de charges hors de la pile.
2.2.2) Donner l’expression de la quantité d’électrons n(e –) échangée lors de la "combustion" de la quantité n(H2) de dihydrogčne dans la pile.
En déduire la valeur de la quantité d’électricité Q échangée.
2.2.3) La pile permet de faire fonctionner correctement la lampe (L) avec une tension ŕ ses bornes de 1,0 V et une intensité constante du courant de 0,70 A.
Déterminer la durée de fonctionnement de la pile pour cette intensité. Commenter ce résultat en comparant cette durée ŕ celle obtenue ŕ la question 1.2.6..
Annexe ŕ rendre agrafée avec la copie
Annexe de l'exercice I
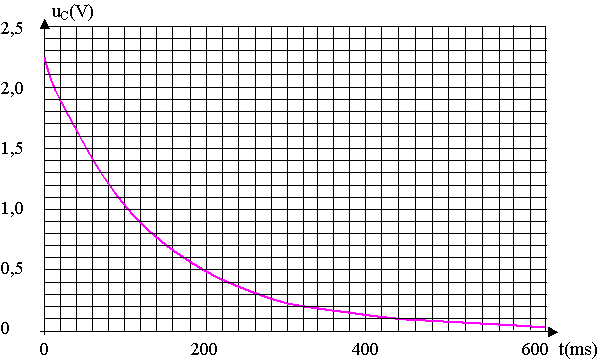
Figure 4 : décharge du condensateur.
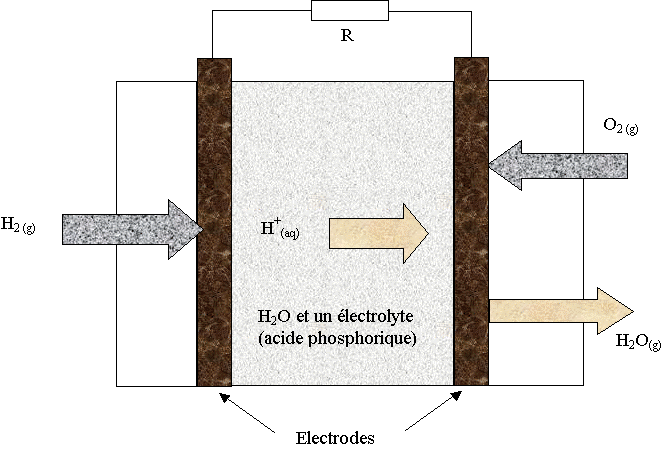
Figure 5 : fonctionnement de la pile ŕ combustible avec un électrolyte acide
©Sciences Mont Blanc
Sujet Bac Nouvelle Calédonie Mars 2008
- II ) Science et sport :
Les parties 1 et 2 de cet exercice sont indépendantes.
Du 13 au 27 juillet 2003 ont eu lieu les dixičmes championnats du monde de natation ŕ Barcelone et parmi les disciplines représentées figurait celle du plongeon. Dans cet exercice on se propose d’étudier, dans un premier temps, le mouvement du centre d’inertie G d’un plongeur, de masse m = 70,0 kg, lors de son saut et dans une deuxičme partie, son évolution dans l’eau.
Dans tout l’exercice le mouvement du centre d’inertie du plongeur est étudié dans le repčre d’axes (Ox, Oy) représenté sur la figure 6.
Le point O est au niveau de la surface de l’eau et l’altitude du centre d’inertie G du plongeur est notée y.
On prendra pour la valeur du champ de pesanteur g = 9,80 m.s –2 et on considčrera que le référentiel terrestre est galiléen.
1) Saut du plongeur
Dans toute cette premičre partie on néglige l’action de l’air sur le plongeur au cours de son mouvement et on admet que lors du saut, les mouvements de rotation du plongeur ne perturbent pas le mouvement de son centre d’inertie G.
On note y0 l’ordonnée du centre d’inertie du plongeur juste avant le saut et v0 sa vitesse initiale.
On donne v0 = 4,0 m.s –1 et y0 = 4,0 m.
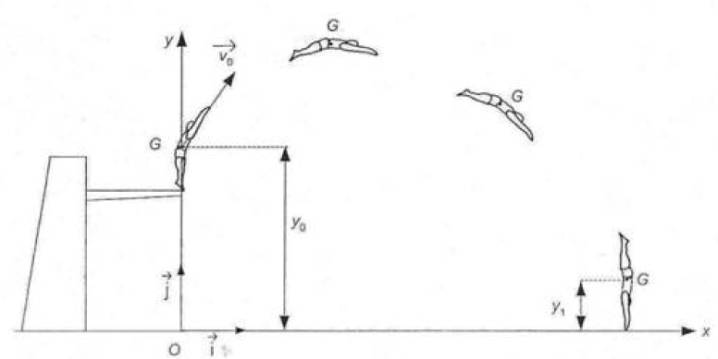
Figure 6
1.1) On considčre le systčme {plongeur} dans le champ de pesanteur terrestre. On a représenté en figure 7, page suivante, l’évolution de l’énergie potentielle de pesanteur du systčme au cours du temps lors d’une partie de la phase de mouvement étudiée. On précise que la référence de l’énergie potentielle Epp est prise au niveau de la surface de l’eau.
On rappelle que, dans ces conditions, l’énergie potentielle de pesanteur du systčme, ŕ l’altitude y, a pour expression : Epp = m . g . y.
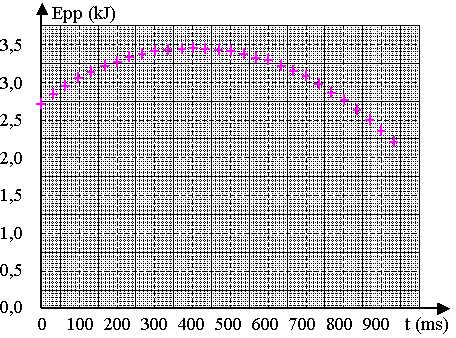
Figure 7
On note tS la date ŕ laquelle l’énergie potentielle de pesanteur est maximale.
En utilisant le graphique ci-dessus déterminer l’altitude yS ŕ laquelle se situe le centre d’inertie G du plongeur ŕ l’instant de date tS.
1.2) Le but de cette question est de déterminer la valeur de la vitesse du centre d’inertie du plongeur au moment oů ses mains touchent l’eau.
1.2.1) Donner l’expression de l’énergie mécanique du systčme {plongeur en interaction avec la Terre} en fonction des grandeurs m, g, y et de la valeur de la vitesse v du centre d’inertie du plongeur.
1.2.2) En justifiant la réponse, dire comment cette énergie évolue au cours du temps.
On rappelle que, dans cette partie, l’action de l’air sur le plongeur est négligée.
1.2.3) Lorsque les mains du plongeur entrent en contact avec l’eau, le centre d’inertie du plongeur se situe ŕ une hauteur y1, au dessus de l’eau (voir figure 6).
A cet instant de date t1 donner l’expression, en justifiant la réponse, de l’énergie cinétique du plongeur en fonction de v0, m, g, y0 et y1.
Calculer sa valeur sachant que y1 = 1,0 m.
1.2.4) En déduire l’expression de la valeur de la vitesse v1 ŕ l’instant de date t1.
Calculer sa valeur.
2) Mouvement dans l’eau
Le mouvement du centre d’inertie G du plongeur est considéré comme vertical dans cette partie.
La profondeur du bassin dans lequel évolue le plongeur est de 5,0 m.
2.1) La figure 8 page suivante, résulte d’une simulation et représente l’évolution de l’altitude y du centre d’inertie du plongeur au cours du temps.
On précise que l’on a pris comme origine des dates l’instant oů le centre d’inertie atteint la surface de l’eau.
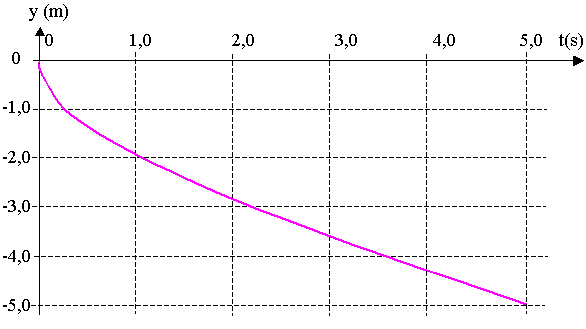
Figure 8
Pour pouvoir remonter, le plongeur doit redresser son buste. On estime que le plongeur agit activement pour amorcer sa remontée 1,0 s aprčs que son centre d’inertie a atteint la surface de l’eau. De plus, on considčre que le centre d’inertie du plongeur se situe toujours ŕ 1,0 m de ses mains tendues.
Au moment oů il amorce sa remontée, les mains du plongeur ont-elles atteint le fond du bassin ? Justifier la réponse.
2.2) On se propose de modéliser le mouvement du centre d’inertie du plongeur dans l’eau s’il n’amorçait pas de remontée. On note V le volume du plongeur et r la masse volumique de l’eau de la piscine. Le plongeur est soumis, entre autres, ŕ une force de frottement fluide dont le sens est opposé celui du vecteur vitesse v et dont la valeur peut ętre modélisée par f = k . v˛ (oů l’on considčre k comme une constante).
2.2.1) Nommer les forces qui s’exercent sur le plongeur lors de ce mouvement.
Les représenter, sans souci d’échelle, en son centre d’inertie G.
2.2.2) En appliquant la deuxičme loi de Newton, montrer que l’équation différentielle qui régit le mouvement du centre d’inertie du plongeur est donnée par :
dvy/dt – (k/m).vy2 + g . (1 - r . V / m) = 0 oů vy est la composante du vecteur vitesse du centre d’inertie sur l’axe vertical orienté vers le haut. On précise que, dans le cas étudié, v = | vy |
2.2.3) En déduire, en la justifiant, l’expression en régime permanent de la valeur vl du vecteur vitesse.
2.2.4) Calculer vl. On prendra r = 1,00 ´ 103 kg.m –3 ; V = 6,50 ´ 10 –2 m3 et k = 150 kg.m-1.
2.2.5) En exploitant la figure 8, dire si le plongeur a atteint le régime permanent avant que ses mains ne touchent le fond.
On rappelle que vy = dy/dt .
2.3) Une méthode de résolution numérique possible, la méthode d’Euler, permet de calculer de façon approchée la valeur algébrique de la vitesse instantanée verticale vy ŕ différentes dates.
On note vy(tn) la valeur algébrique de la vitesse ŕ l’instant de date tn ; la valeur algébrique vy(tn+1) ŕ la date tn+1 = tn + Δt est calculée en utilisant la relation (1) suivante :
vy(tn+1) = vy(tn) + ay(tn).Δt
oů ay = dvy/dt est la composante de l’accélération selon l’axe (Oy) et Δt est le pas de calcul.
Compte tenu des valeurs numériques , l’équation différentielle obtenue en 2.2.2. permet d’obtenir la relation (2) suivante :
ay(t) = 2,14 x vy2(t) – 0,700
La valeur du pas de calcul Δt sera choisie égale ŕ la durée Δt = 1,20 ´ 10 –2 s.
En utilisant la relation (1) pour le calcul de vy(tn+1) et la relation (2) pour celui de ay(tn), compléter avec des valeurs numériques le tableau 1.
Tableau 1 :
|
Dates en s |
vy en m.s-1 |
ay en m.s-2 |
|
tn = 1,44 ´ 10 –1 |
vy(tn) = – 2,21 |
ay(tn) = 9,75 |
|
tn+1 = 1,56 ´ 10 –1 |
vy(tn+1) = ……. |
ay(tn+1) = ……. |
|
tn+2 = 1,68 ´ 10 –1 |
vy(tn+2) = –1,99 |
ay(tn+2) = 7,77 |
©Sciences Mont Blanc
Sujet Bac Nouvelle Calédonie Mars 2008 - III ) Un conservateur
alimentaire :
L'acide benzoďque est un conservateur utilisé dans de nombreux cosmétiques et produits pharmaceutiques. Il est naturellement présent dans le propolis (sous-produit du miel) et dans les canneberges (arbustes ŕ baies rouges comestibles).
Il est aussi souvent utilisé comme conservateur (E 210) dans certains aliments tels que les jus de fruits.
L'acide benzoďque et ses sels (benzoate de sodium ou de potassium) sont efficaces contre les levures et ŕ un moindre degré, contre les moisissures.
Ils sont peu actifs contre les bactéries mais agissent tout de męme sur les bactéries lactiques.
La solubilité d'une espčce chimique représente, ŕ une température donnée, la quantité de matičre maximale de cette espčce que l'on peut dissoudre par litre de solution. Il s'agit ici d'étudier l'évolution de la solubilité de l'acide benzoďque C6H5CO2H(s) dans l'eau en fonction de la température.
La solubilité de l'acide benzoďque dans l'eau augmente quand la température augmente.
Cette propriété est utilisée dans un procédé de purification des produits : la recristallisation.
Données : Masse molaire moléculaire de l'acide benzoďque M = 122 g.mol –1
Conversion de degré celsius en kelvin : T(K) = θ(°C) + 273
1) Composition d'une solution saturée d'acide benzoďque
L'acide benzoďque se présente ŕ l'état pur sous la forme de cristaux blancs.
La dissolution de l'acide benzoďque dans l'eau se traduit par l'équation suivante :
C6H5CO2H(s) = C6H5CO2H(aq)
Une solution saturée est obtenue lorsque l'acide benzoďque solide reste présent dans la solution.
A 24°C, on peut dissoudre au maximum 3,26 g d'acide benzoďque par litre de solution.
1.1) L'acide benzoďque appartient au couple acido-basique C6H5CO2H(aq)/C6H5CO2-(aq).
Ecrire l'équation de la réaction entre l'acide benzoďque et l'eau.
1.2) Déterminer la concentration molaire apportée c dans un litre de solution saturée d'acide benzoďque ŕ 24°C.
En déduire en utilisant la définition donnée dans le texte, la valeur de la solubilité s de l'acide benzoďque ŕ 24°C exprimée en mol.L –1.
1.3) Déterminer l'avancement maximal de la réaction de l'acide benzoďque avec l'eau dans un volume de 20,0 mL de solution saturée.
On pourra s'aider d'un tableau d'avancement.
1.4) Le pH de cette solution vaut 2,9. Déterminer l'avancement final puis le taux d'avancement final de la réaction.
La transformation correspondante est-elle totale ?
1.5) Choisir, en justifiant, la conclusion adaptée parmi les deux suivantes :
(a) dans une solution saturée d'acide benzoďque ŕ l'équilibre, la concentration en ion benzoate est sensiblement égale ŕ la concentration en acide benzoďque.
(b) dans une solution saturée d'acide benzoďque ŕ l'équilibre, la concentration en acide benzoďque dans la solution ŕ l'équilibre est sensiblement égale ŕ la concentration apportée en acide benzoďque.
2) Titrage des solutions saturées d'acide benzoďque
Plusieurs solutions saturées d'acide benzoďque sont préparées selon le protocole suivant :
- A une masse de 0,55 g d'acide benzoďque placée dans un erlenmeyer, ajouter 100 mL d'eau distillée.
- Chauffer au bain-marie afin de dissoudre l'acide benzoďque.
- Refroidir sous courant d'eau froide jusqu'ŕ une température supérieure de 5°C ŕ la température θ souhaitée.
- Verser le contenu de l'erlenmeyer dans un bécher thermostaté ŕ la température θ.
Attendre que la température se stabilise.
- Prélever un volume Vp = 20,0 mL de solution surnageante.
Placer cette solution dans un bécher thermostaté.
Différentes solutions saturées d'acide benzoďque sont ainsi obtenues ŕ différentes températures θ allant de 24°C ŕ 50°C.
Chacune des solutions est titrée par une solution d'hydroxyde de sodium de concentration cb = 5,0 ´ 10 –2 mol.L –1 ; le volume titré est Vp = 20,0 mL.
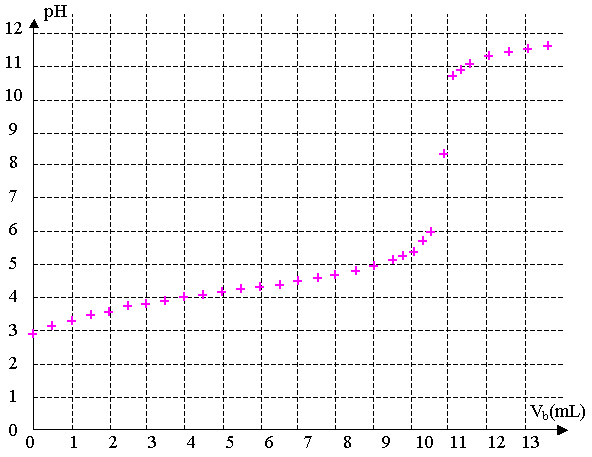
On s'intéresse ici au titrage de la solution obtenue ŕ 24°C. La courbe obtenue lors de ce titrage donnant l’évolution du pH en fonction du volume Vb d'hydroxyde de sodium versé est représentée sur la figure 9 de l’Annexe.
2.1) Ecrire l'équation de la réaction modélisant la transformation ayant lieu lors du titrage de l'acide benzoďque.
2.2) Définir l'équivalence du titrage.
2.3) Déterminer par une méthode graphique que l'on fera apparaître sur la figure 9 de l'Annexe le volume VbE de solution d'hydroxyde de sodium versé ŕ l'équivalence.
2.4) Calculer la concentration molaire c d'acide benzoďque dissous dans la solution.
En déduire la valeur de la solubilité de l'acide benzoďque ŕ 24°C.
2.5) En déduire la masse maximale d'acide benzoďque que l'on peut dissoudre
dans 100 mL de solution ŕ 24°C.
Comparer cette masse ŕ celle introduite initialement et expliquer alors l'expression "solution saturée" employée.
3) Variation de la solubilité de l'acide benzoďque dans l'eau en fonction de la température
Les valeurs des solubilités des différentes solutions ont été mesurées suivant la męme méthode, puis traitées par un tableur grapheur.
La figure 10 représente l'évolution de la solubilité s en fonction de la température T exprimée en kelvin.
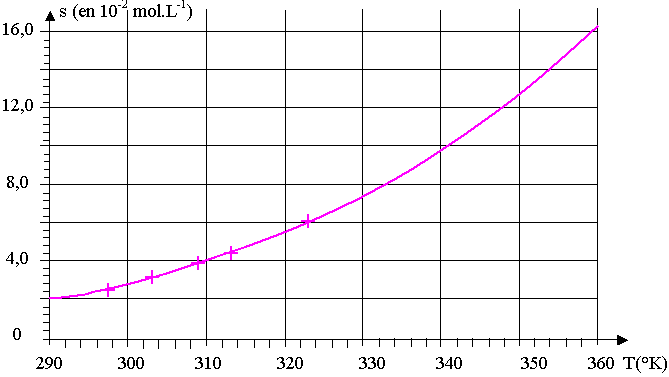
Figure 10
3.1) Parmi les quatre équations proposées ci-dessous, une seule peut modéliser la courbe de la figure 10. Choisir l'expression correcte. Justifier.
(1) s = a . T + b ; (2) s = b . e – a . T ; (3) s = b . e – a / T ; (4) s = a / T + b ; a et b étant des constantes positives.
3.2) A l'aide de la figure 10, déterminer la valeur de la solubilité de l'acide benzoďque s ŕ une température de 80°C.
Annexe de l'exercice III
©Sciences Mont Blanc