Correction Bac Pondichéry Mars 2008
Calculatrice autorisée
I ) Propriétés des solutions d'ammoniac (7 points)
II ) Quelques propriétés du plutonium (5 points)
III ) Mesure de la valeur de la capacité d'un condensateur (4 points)
III (spe) Quelques propriétés de la flûte de pan (4 points)
Correction Bac Pondichéry Mars 2008 - I ) Propriétés des solutions d'ammoniac :
1.1) Préparation de la solution diluée S :
On veut préparer 1,0 L de solution CS .
Lors d'une dilution, la quantité de matičre ne change pas : n(avant) = n(aprčs) ( on ne rajoute que de l'eau)
C0 .V0 = CS.VS ; V0 = VS. CS / C0 = 1000 / 100 = 10 mL
On prélčve 10 mL de solution mčre S0 avec une pipette jaugée et une propipette.
On la verse dans une fiole jaugée de 1,0 L que l'on complčte avec de l'eau distillée.
On la bouche et on reourne plusieurs fois pour homogénéiser la solution.
1.2) Titrage de la solution diluée S :
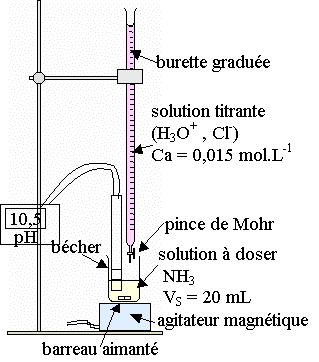
1.2.1) schéma légendé du dispositif de titrage.
1.2.2) Réaction de titrage :
H3O+(aq) + NH3 (aq) → NH4+(aq) + H2O(l)
1.2.3) Détermination des concentrations :
a) On peut utiliser la méthode des tangentes mais elle est moins précise que la méthode de la dérivée.
La dérivée dpH/dVa prend une valeur maximale (en valeur absolue) ŕ l'équivalence.
D'aprčs la courbe dpH/dVa , VaE = 14 mL ( il est difficile d'ętre plus précis)
b) A l'équivalence, les réactifs sont complčtement consommés :
n(H3O+ )f = 0 = n(H3O+ )E – xmax ; xmax = n(H3O+ )E = Ca . VaE
n(NH3)f = 0 = n(NH3)0 – xmax ; xmax = n(NH3)0 = CS . VS
xmax = n(H3O+ )E = n(NH3)0 ; Ca . VaE = CS . VS
CS = Ca . VaE / VS = 0,015 x 14.10-3 / 20.10-3 = 0,0105 mol.L-1
C0 = 100 CS = 100 x 0,0105 = 1,05 mol.L-1
Cette valeur est trčs proche de celle de l'énoncé de 1,1 mol.L-1
1.2.4) D'aprčs la courbe pH = f(Va), le pH ŕ l'équivalence pHE est proche de 6.
L'indicateur le plus adapté est celui pour lequel, pHE est compris dans la zone de virage. On choisit donc le rouge de méthyle .
1.3.1) a) K = [NH4+]éq . [HO-]éq / [NH3]éq
1.3.1) b) On multiplie en haut et en bas par [H3O+] :
K = ([H3O+]éq . [HO-]éq ) .[NH4+]éq . / ([NH3]éq . [H3O+]éq) = Ke / KA2 = 10-14 / 10-9,2 = 1,6.10-5
1.3.2) a)
|
Equation |
NH3 (aq) + H2O( l) = NH4+(aq) + HO–(aq) |
||||
|
Etat |
Avancement (mol) |
Quantité de matičre (mol) |
|||
|
Etat initial |
0 |
n(NH3)i |
Excčs |
0 |
0 |
|
Etat final |
xéq |
n(NH3)i - xéq |
Excčs |
xéq |
xéq |
1.3.2.b) K = [NH4+]éq . [HO-]éq / [NH3]éq = n(NH4+)éq . n(HO-)éq / (US . n(NH3)éq)
n(NH3 )éq = n(NH3)i - xéq ≈ n(NH3)i ≈ CS . US ; n(NH4+)éq = n(HO-)éq = xéq
On a donc : K ≈ xéq2 / (CS.US2)
1.3.2.c) xéq2 = K . CS . US2 ; xéq
= US .  (K . CS
)
(K . CS
)
xéq = 1,0 x  (1,6.10-5
x 1,1.10-2 ) = 4,2.10-4 mol
(1,6.10-5
x 1,1.10-2 ) = 4,2.10-4 mol
CS . US = 1,1.10-2 x 1,0 = 1,1.10-2 ; xéq est donc bien négligeable devant CS . US .
1.3.3) Etude conductimétrique :
La valeur de la conductivité de la solution diluée S est σ = 8,52.10–3 S.m-1.
1.3.3.a) σ = λ(NH4+ ) . [NH4+] + λ(HO-) . [HO-] = (λ(NH4+ ) + λ(HO-)) . [NH4+]
[NH4+ ] = [HO-] = σ / (λ(NH4+ ) + λ(HO-)) = 8,52.10-3 / (73,4 + 199).10-4 = 0,313 mol.m-3
[NH4+ ] = [HO-] = 3,13.10-4 mol.L-1
1.3.3.b) [H3O+] = Ke / [HO-] = 10-14 / 3,13.10-4 = 3,2.10-11 ; pH = - log [H3O+] = 10,5
D'aprčs le graphique du pH en fonction de Va, le pH de la solution S correspond ŕ Va = 0 mL et il est proche de 10,5.
©Sciences Mont Blanc
Correction Bac Pondichéry Mars 2008 - II
) Quelques propriétés du plutonium :
©Sciences Mont Blanc
Correction Bac Pondichéry Mars 2008 - III ) Mesure
de la valeur de la capacité d'un condensateur :
©Sciences Mont Blanc
Correction Bac Pondichéry Mars 2008 - III
) Quelques propriétés de la flûte de pan (spécialité)
:
©Sciences Mont Blanc
