Correction Bac Afrique Juin 2011
Calculatrice autorisée
II ) Chimie au quotidien (5,5 points)
III ) Le laser au quotidien
(4 points)
III )(spe) La physique du vide grenier
(4 points)
Afrique Juin 2011 - I ) Les curie
1.1.) Un Becquerel correspond ŕ une désintégration par seconde.
1.2.1.) Z = 88 .
Le noyau contient donc 88 protons.
N = A – Z = 226 – 88 = 138.
Le noyau contient donc 138 neutrons.
1.2.2.) On utilise les lois de conservation de Soddy :
Conservation
du nombre de charge : 88 = Z + 86
; Z = 2.
Conservation du nombre de masse :
226 = A + 222 ; A = 4.
Le noyau formé est donc une particule α, un noyau d’hélium 42 He.
Equation : 22688 Ra → 22286 Ra
+ 42 He + γ
1.2.3.) Le noyau de radon est produit ŕ l’état excité . Lorsqu’il se désexcite, il émet un rayonnement γ.
1.3.) Δm = m(22286Rn)
+ m(42He) – m(22688Ra) = 221,9703
+ 4,00150 – 225,9791 = - 7,3 x 10-3 u
Δm = - 7,3 x 10-3 x 1,66606 x 10-27 = - 1,22 x 10-29 kg
E = Δm x c2 = - 1,22 x 10-29 x (3,00 x 108)2 = - 1,09 x 10-12 J
1.4.1.) N = m
/ m(radium) = 1,00 x 10-3 (kg) / (225,9791 x 1,66606 x 10-27 ) = 2,66 x 1021 noyaux
1.4.2.)
λ = A / N = 3,70 x 1010 / 2,66 x 1021 = 1,39 x 10-11 s-1
t ˝ = ln 2 / λ = ln 2 / 1,39 x 10-11 = 4,98 x 1010 s
t ˝ = 4,98 x 1010 / ( 60 x 60 x 24 x 365,25 ) = 1577 ans ≈ 1,58 x 103 ans
1.4.2.) N(t1) = N0 – 3 N0 / 4 = N0 / 4 ; N(2 t ˝ ) = N(t ˝ ) / 2 = N0 / 4
t1 = 2 t ˝ = 2 x 1,58 x 103 = 3,15 x 103 ans
2.1.1. ) La radioactivité naturelle est spontanée, elle se produit sans intervention extérieure. La radioactivité artificielle est provoquée en bombardant les noyaux cibles par des particules.
2.1.2. ) Des isotopes sont des noyaux de męme numéro atomique Z, de męme nom mais un nombre de neutrons différent.
Les deux noyaux de phosphore ont 15 protons , le phosphore 31 a 16 neutrons et le phosphore 30 en a 15 . Ils sont bien isotopes.
2.2.1. ) Lors d’une désintégration β+, la particule émise est un positon 0+1e.
2.2.2. ) On utilise les lois de conservation de Soddy :
Conservation
du nombre de charge : 14 = Z + 1 ;
Z = 1.
Conservation du nombre de masse :
30 = A + 0 ; A = 30
Equation : 3015P → 3014Si + 0+1e
2.2.3.) Il n’y a pas d’émission de rayonnement car le silicium
30 est obtenu non excité, dans son état fondamental.
©Sciences Mont Blanc
Afrique Juin 2011 - II ) Chimie au quotidien
1.1.1.) La tension ŕ vide d'un dipôle est la f. e. m. , force électromotrice.
1.1.2.) La borne V du voltmčtre est reliée ŕ la pičce , la tension obtenue étant positive, cette borne est le pôle + de la pile. Le trombone est la borne - .
1.2.1.) Le gaz dihydrogéne est testé en approchant une flamme. Il se produit une détonation avec un bruit nommé « cri du chien ».
1.2.2.) La borne négative de la pile fournit des électrons ŕ l'horloge, il s'y produit une oxydation : Zn (s) = Zn2+(aq) + 2 e- Le trombone est l'anode.
A la borne positive , se produit une réduction :
2 H+(aq) + 2
e- = H2 (g)
La pičce en cuivre est la cathode.
1.2.3.) Le nombre d'électrons étant le męme , on ajoute les 2 demi-équations : 2 H+(aq) + Zn(s) = H2 (g) + Zn2+(aq)
1.2.4.) Le jus de citron est une solution contenant de l'acide citrique, qui réagit en formantdes ions H+.
1.2.5.) Le vinaigre et le jus d'orange sont des solutions
acides.
Elles auraient pu remplacer le jus de citron.
1.2.6.) Pour obtenir une tension ŕ vide 2 fois plus grande, il faut utiliser deux piles branchées en série.
1.3.1.) Δt = 5 min 30 s ; I = 10 mA = 0,010 A , Q = I x Δt = (5 x 60 + 30) x 0,010 = 3,3 C
1.3.2.) D'aprčs la demi-équation, 2 n(Zn)cons = n(e-)
Q = n(e-) x F = 2 n(Zn)cons x F ; n(Zn)cons
= Q / 2 F = 3,3 / (2 x 96 500) = 1,7.10-5 mol
1.3.3.) Δm = mfinale - minitiale = - mconsommée = - n x M(Zn) = - 1,7.10-5 x 65,4 = - 1,1.10-3 g
2.1.1.) n(Cu2+)
= c x V = 1,0 x 0,250 = 0,25 mol = n(CuSO4)
m(CuSO4) = n x M(CuSO4) = 0,25 x (63,5 + 32,1 + 4 x
16,0) = 40 g
m = m(CuSO4) / 0,80 = 40 / 0,80 = 50 g
2.1.2. ) On pčse 50 g de bouillie bordelaise avec une balance que l'on verse dans une fiole jaugée de 250 mL.
On remplit environ 2/3 du volume avec de l'eau distillée et on agite pour dissoudre le solide.
On complčte avec de l'eau distillée jusqu'au trait de jauge et on retourne plusieurs fois pour homogénéiser la solution.
2.2.1. ) Cu2+(aq) + 2 e- = Cu(s) réduction Fe(s) = Fe2+(aq) + 2 e- oxydation
Cu2+(aq)
+ Fe(s) = Cu(s) + Fe2+(aq)
oxydant , réducteur
2.2.2 . ) Q r, i = [Fe2+]i / [Cu2+]i = 0 on suppose qu'il n'y a pas d'ions Fe2+ dans la bouillie bordelaise.
Q r, i << K . D'aprčs le critčre d'évolution spontanée ; la réaction évolue dans le sens direct de la formation du métal cuivre
2.2.3 ) Pour qu'il y ait réaction, il faut un contact entre les ions Cu2+ et le métal fer.
La couche de cuivre empęche ce contact et arręte la réaction.
2.3.1.) Le dépôt de cuivre doit se faire sur la clé. Cu2+(aq) + 2 e- = Cu(s) réduction ŕ la cathode
2.3.2.) Réaction ŕ la pičce de cuivre : Cu(s) = Cu2+(aq) + 2 e- oxydation ŕ l’anode
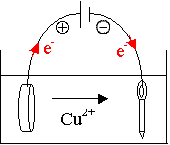 En les ajoutant, on obtient : Cu2+(aq)
+ Cu(s) pičce = Cu(s) clé + Cu2+(aq)
En les ajoutant, on obtient : Cu2+(aq)
+ Cu(s) pičce = Cu(s) clé + Cu2+(aq)
2.3.3.) La borne - de la pile fournit les électrons au circuit, ŕ la clé pour réduire Cu2+ en Cu. On relie donc la clé ŕ la borne -.
©Sciences Mont Blanc
Afrique Juin 2011 - III ) Le laser au quotidien
1.1.) La diffraction de la lumičre crée l’irisation d’un CD ou DVD.
1.2.) c = λ / T = λ x ν ; νB = c / λB = 3,00 x 108 / (405 x 10-9 ) = 7,41 x 1014
Hz
1.3.) La longueur d’onde d’un DVD est supérieure ŕ 405 nm car sa couleur est rouge. Celle d’un CD est supérieure ŕ 800 nm car c’est une lumičre I.R. .
2.1.1. ) tan θ = côté opposé / côté adjacent = ( L / 2 ) / D = L / 2 D
tan θ ≈ θ . θ = L / 2 D.
2.1.2. ) θ = λD / a avec λD et a en mčtre .
2.1.3. )
λD / a = L / 2 D ; λD = L x a / 2 D
2.2. ) λD / L = a / 2 D = λB / L’ ; λD = λB x L / L’ = 405 x 4,8 / 3,0 = 648 nm = 6,5 x 102
nm
Cette valeur est bien supérieure ŕ 405 nm et correspond ŕ celle des lasers rouges utilisées en T.P.
3.1.) n = c / v
3.2.) La fréquence du laser n’est pas modifiée lors d’un changement de milieu.
3.3.1.) c = λ x ν ; v = λC x ν ; ν = c / λ = v / λC ; n = c / v = λC / λ ; λC = λ / n
3.3.2.) λC = 780 / 1,55 = 503 nm
©Sciences Mont Blanc
Afrique Juin 2011 - III ) La physique du vide
grenier (spe):
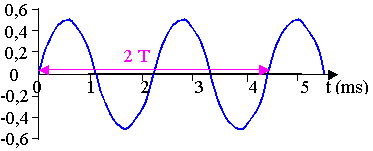
1.1.1. ) 2 T = 4,4
ms ; T = 2,2 ms ; f = 1 / T = 1 / (2,2 x 10-3 ) = 455 Hz
1.1.2. ) Le signal obtenu est sinusoďdale.
1.2.1. ) La
figure 2 montre que l’enveloppe de US correspond au signal modulant,
la modulation est donc satisfaisante.
1.2.2. ) m = um
/ E = 0,5 / 2 = 0,25
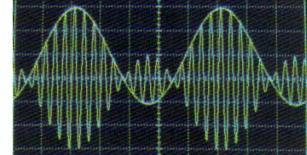 1.2.3.
) En cas de surmodulation, l’enveloppe ne correspond plus au signal modulant.
1.2.3.
) En cas de surmodulation, l’enveloppe ne correspond plus au signal modulant.
1.3.1. ) F2
= F + f ; F1 = F -
f
1.3.2. ) Δf = F2 – F1 = 2 f = 2 x 440 = 880 Hz
2.1.1. ) Pour capter le signal , il faut régler la fréquence sur celle de la porteuse , f0 = 164 kHz
2.1.2. )
f0 = 1 / ( 2 π ![]() (L
x C ) ; f02 x 4 π2 = 1 / ( L x C ) ; C = 1 / ( L x f02 x 4 π2 )
(L
x C ) ; f02 x 4 π2 = 1 / ( L x C ) ; C = 1 / ( L x f02 x 4 π2 )
C = 1 / ( 2,0
x 10-3 x ( 164 x 103 x 2 x 3,14 )2 ) = 4,7
x 10-10 F = 0,47 nF
2.1.3. ) Le bouton sélection des stations permet de régler
mécaniquement la valeur de la capacité C du condensateur et donc de régler
la fréquence f0 = 1 / ( 2 π ![]() (L x C ) du poste radio.
(L x C ) du poste radio.
2.2.1. )
[R’.C’] = [uR / i] x [Q /uC] = (U / I ) x [ I x t /
uC ] = (U / I ) x ( I x T / U ) = T
R’ . C’ est bien homogčne ŕ un temps.
2.2.2. )
Tm = 1 / f = 1 / (1,0 x 103 ) = 1,0 x 10-3 s =
1,0 ms
TP = 1 / fP = 1 / (164 x 103 ) = 6,10 x 10-6 s
C’1 = 50 pF , τ1’ = 15 x 103 x 50 x 10-12 = 7,5 x 10-7 s < TP . Cela ne convient pas.
C’2
= 50 nF , τ2’
= 15 x 103
x 50 x 10-9 = 7,5 x 10-4 s = 0,75 ms.
TP << τ2’ < Tm . Cela convient .
C’3 = 50 μF , τ3’ = 15 x 103 x 50 x 10-6 = 7,5 x 10-1 s > Tm . Cela ne convient pas.
On choisit donc la capacité de 50 nF.
©Sciences Mont Blanc
