Correction Bac Antilles Juin 2011
Calculatrice autorisée
I ) Le Luminol. Au service de la police scientifique( 6,5 points)
II ) Pile au lithium et super condensateur ( 5,5 points)
III ) Radars ... et effet Doppler ( 4 points)
III ) Science appliquée (spe) ( 4 points)
Correction Antilles Juin 2011- I ) Le Luminol. Au service
de la police scientifique :
1. La lumičre émise est une lumičre bleue.
1.1.1. Une onde lumineuse appartient au domaine électromagnétique.
1.1.2. Une onde mécanique a besoin d’un milieu matériel pour se propager alors qu’une onde lumineuse se propage dans un milieu transparent dont le vide.
1.2.1. E = h x
ν = h x c / λ = 6,63.10-34 x 3,0.108
/ 400.10-9 = 5,0.10-19 J
1.2.2. Si la lumičre émise est rouge ; sa longueur d’onde est supérieure ŕ 400 n. Leur célérité est la męme. L’énergie correspondante est donc plus faible.
2. La réaction produite est une réaction d'oxydoréduction.
L'équation de la réaction s'écrit :
2 C8H7N3O2
(aq) + 7 H2O2
(aq) + 4 HO –
(aq) = 2 N2 (g) + 2 C8H2O42–
(aq) + 14 H2O (l)
2.1. Un oxydant est une espčce chimique capable de capter un ou plusieurs électrons.
2.2.1. MnO4– (aq) + 5 e- + 8 H+(aq) = Mn2+(aq) + 4 H2O(l) ) x 2
H2O2
(aq). = O2
(aq) + 2 H+(aq)
+ 2 e- )
x 5
équation : 2 MnO4– (aq) + 16 H+(aq) + 5 H2O2 (aq). = 5 O2 (aq) + 10 H+(aq) + 2 Mn2+(aq) + 8 H2O(l)
2 MnO4– (aq) + 6 H+(aq) + 5 H2O2 (aq). = 5 O2 (aq) + 2 Mn2+(aq) + 8 H2O(l)
2.2.2. A l'équivalence, les réactifs ont été ajoutés dans les proportions stoéchiométriques de l’équation. Leurs quantités finales sont nulles.
Au début du dosage, le mélange est incolore car les ions MnO4- violets réagissent et sont consommés Juste aprčs l’équivalence ; ils restent dans le mélange, la solution vire au violet.
2.2.3.
|
Equation |
2 MnO4– (aq) + 6 H+(aq) + 5 H2O2 (aq). = 5 O2 (aq) + 2 Mn2+(aq) + 8 H2O(l) |
|||
|
Etat final |
n1 – 2 xmax |
excčs |
n2 – 5 xmax |
|
Les réactifs sont limitants : n1 – 2 xmax = 0 ; xmax = n1 / 2 ; n2 – 5 xmax = 0 ; xmax = n2 / 5
n1 / 2 = n2 / 5 ; 5 n1 = 2 n2 : n1 = c0 x VE ; n2 = cR x VR ; 5 c0 x VE = 2 cR x VR
cR
= 5 c0 x VE / ( 2 VR ) = 5 x 0,50 x 8,0.10-3
/ ( 2 x 10,0.10-3 ) = 1,0 mol.L-1
L’eau oxygénée est diluée dix fois. C
= 10 cR = 10 mol.L-1 .
Cette valeur est bien voisine de 9,8 mol.L-1
3. La réaction entre le luminol et l'eau oxygénée est une transformation lente.
3.1.1. P0 x Vgaz = n(air) x R x T ; P0 = n(air) x R x T / Vgaz
3.1.2. P x Vgaz = (n(air) + n(N2) ) x R x T ; P = (n(air) + n(N2) ) x R x T / Vgaz
3.1.3. P – P0 = n(N2) x R x T / Vgaz
3.2.
|
Avancement |
2 C8H7N3O2 (aq) + 7 H2O2 (aq) + … = 2 N2 (g) + … |
|||
|
État initial |
0 |
n1 = 5,6.10–3 mol |
n2 = 4,9.10–3 mol |
0 |
|
État intermédiaire |
x |
n1 – 2 x |
n2 – 7 x |
2 x |
|
État
final |
xmax |
n1
– 2 xmax |
n2
– 7 xmax |
2 xmax |
Si le luminol est en défaut, nf = 0 = n1 – 2 xmax ; xmax = n1 / 2 = 5,6.10-3 / 2 = 2,8.10-3mol
Si H2O2 est en défaut, nf = 0 = n2 – 7 xmax ; xmax = n2 / 7 = 4,9.10-3 / 7 = 7,0.10-4 mol
On choisit la plus petite valeur de xmax atteinte en 1er . xmax = 7,0.10-4 mol et H2O2 est limitant.
3.3. D’aprčs le tableau, x = n(N2) / 2 = (P – P0) x Vgaz, / (R x T )
3.4. xmax = ( 1660 x 2,1.10-3) / (2 x 8,3 x 300 = 7,0.10-4 mol ( Attention Vgaz doit ętre en m3 )
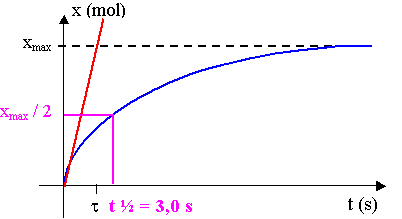
3.5.1. La vitesse volumique de réaction est proportionnelle au coefficient directeur de la tangente ŕ la courbe.
D’aprčs le graphique, elle est maximale au départ, puis elle diminue jusqu’ŕ s’annuler.
Cette diminution de la vitesse est due ŕ la diminution des concentrations des réactifs (facteur cinétique)
3 5.2. Le temps de demi-réaction t1/2 est la durée au bout de laquelle x vaut xmax / 2.
D’aprčs le graphique, t ˝ = 3,0 s
4. La réaction entre le luminol et l'eau oxygénée devient rapide en présence d'un composé ferrique.
4.1. Un catalyseur est une espčce chimique qui accélčre la réaction sans la modifier.
4.2. Sur une scčne de crime, la police scientifique cherche
ŕ détecter les traces de sang. En utilisant le mélange luminol-eau oxygénée
sur une zone, l’apparition de la couleur bleue montre la présence des ions
Fe3+ car sans sa présence, la couleur n’apparaît, la réaction est
trop lente, on voit ainsi les traces de sang lŕ oů il y a des traces bleues.
©Sciences Mont Blanc
Correction Antilles Juin 2011- II ) Pile au
lithium et super condensateur :
©Sciences Mont Blanc
Correction Antilles Juin 2011 - III ) Radars ... et effet
Doppler :
©Sciences Mont Blanc
Correction Antilles Juin 2011 - III ) Science appliquée
(spe) :
©Sciences Mont Blanc