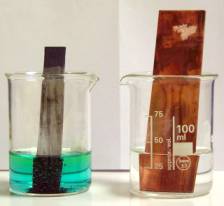1eS - Chap 07 - RÈactions d'oxydo-réduction![]()
I ) La rÈaction rÈdox :
1) ExpÈriences :
|
|
|
||
|
lame de zinc dans une solution (Cu2+, SO42-) |
lame de cuivre dans une solution (Zn2+, 2Cl-) |
du mÈtal cuivre se forme sur la lame |
rien ne se passe |
Les ions cuivre Cu2+ sont consommÈs et du mÈtal cuivre se forme. Il s'agit d'une rÈduction.
Les ions cuivre gagnent 2 Èlectrons pour devenir des atomes†† :†† Cu2+(aq)† +† 2 e-† →† Cu(s)
Le mÈtal zinc est attaquÈ et des ions zinc Zn 2+ se forment. Il s'agit d'une oxydation.
Les atomes de zinc cËdent 2 Èlectrons pour devenir des ions Zn2+ :††† Zn(s)† →† Zn 2+(aq) + 2 e-
Par contre , les ions zinc Zn 2+ ne rÈagissent pas avec le mÈtal cuivre.
2) DÈfinition :
Une rÈaction rÈdox est caractÈrisÈe par un transfert díÈlectrons entre deux espËces chimiques, líune Ètant appelÈe líoxydant et líautre le rÈducteur.
3)
 Oxydation
et rÈduction :
Oxydation
et rÈduction :
Une oxydation est une perte díÈlectrons
Une rÈduction est un gain díÈlectrons.
ExpÈrience de líarbre de Diane : on plonge du mÈtal cuivre dans une solution de nitrate d'argent.
Le mÈtal argent se dÈpose sur le mÈtal cuivre et la solution
devient bleue indiquant la prÈsence d'ions cuivre Cu2+
Le rÈducteur qui subit une oxydation et líoxydant qui subit une rÈduction .
Le rÈducteur est une espËce capable de donner un ou plusieurs Èlectrons.
Líoxydant est une espËce qui capte un ou plusieurs Èlectrons.
Líoxydation díune espËce chimique et la rÈduction díune autre se font toujours simultanÈment : on parle alors de rÈaction rÈdox.
II ) Couple oxydant : rÈducteur :
1) DÈfinition :
Une espËce chimique oxydante et une espËce rÈductrice forment un couple oxydant / rÈducteur (ou couple rÈdox) si líon peut passer de líun ‡ líautre par gain ou perte díun ou plusieurs Èlectrons.† Le couple est alors notÈ Ox / RÈd ( oxydant ‡ gauche ) et les espËces sont dites conjuguÈes.
exemples :†† Cu2+(aq) / Cu(s)†† et† Ag+(aq) / Ag(s)
2) Demi-Èquation associÈe ‡ un couple :
Selon les conditions expÈrimentales, on peut observer la transformation :
†††††††† Ox† +† n.e-† →† Red††††††††† ou††††† †Red† → Ox† +† n.e-†
Attention , les Èlectrons e-† sont toujours du cÙtÈ de líoxydant
Pour symboliser le fait que ces 2 transformations sont possibles, on associe ‡ un couple rÈdox une demi-Èquation :†††† Ox† +† n† . e-† =† Red
exemple ÈtudiÈ dans les expÈriences :†††† Cu2+(aq) + 2 e- = Cu(s)†††
3) Equation globale de la rÈaction :
Si un oxydant Ox1 rÈagit de faÁon spontanÈe sur un rÈducteur RÈd2 , on Ècrit les demi-Èquations de la rÈduction de Ox1 et de l'oxydation de Red1 :
Ox1† +† n1 . e-† =† Red1††††††† et †††††††Red2† = Ox2† +† n2 .e-
Les Èlectrons sont cÈdÈs par Red2 et captÈs par Ox1. Il faut donc que le nombre d'Èlectrons mis en jeu par l'oxydation soit identique ‡ celui de la rÈduction.
On multiplie la demi-Èquation de la rÈduction par n2 et celle de l'oxydation par n1 et on les ajoute.
n2 x† ( Ox1† +† n1 . e-† =† Red1 )†††††† et†††††† n1 x († Red2† = Ox2† +† n2 .e-† )
Bilan :† n2 Ox1† + n1 Red2† =† n2 Red1† +† n1 Ox2
Exemple : arbre de Diane :†††††††
Cu(s)† =†† Cu2+(aq)† + 2 e-†††††††† et†††††††† ††††††† 2 x († Ag+(aq)† + e-† =† Ag(s)† )
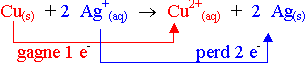
Bilan :† Cu(s)† +† 2 Ag+(aq)† =† Cu2+(aq) +† 2 Ag(s)
III ) Exemples de couples rÈdox :
1) Couple cation mÈtallique / mÈtal :
Exemples :††† Cu2+(aq)† / Cu(s)††††††††††††† Ag+(aq) / Ag(s)††††††††††††††††† Pb2+(aq) / Pb(s)
2) Couple formÈ par 2 cations mÈtalliques :
Exemples :†† Fe3+(aq)† / Fe2+(aq) †††††††††††††††††††† Fe3+(aq)† +† e-†† =†† Fe2+(aq)†
†††††††† Cu2+(aq) / Cu+(aq)††††††††††††††††††††††† Cu2+(aq)† + e-†† = Cu+(aq)†
3) Couple formÈ díun ion et díune molÈcule :
Exemples :†† †††††††† H+(aq) / H2 (g)††††††††††††††††††† 2 H+(aq) + 2 e-† =† H2 (g)†
†††††††††††††††††† I2 (aq)† /† I-(aq)††††††††††††††††††† I2 (aq)† +† 2 e-†† =† 2 I-(aq)†
4) Couples dans lesquels un ÈlÈment commun síassocie ‡ líoxygËne :
* couple :† MnO4-(aq)† /† Mn2+(aq)†† ( ion permanganate violet† / ion manganËse incolore)
MnO4-(aq)† est un oxydant en milieu acide :†† MnO4-(aq)† + 8 H+(aq) + 5 e-† =† Mn2+(aq)† + 4 H2O(l)
†
* couple :† S4O62-(aq)† /† S2O32-(aq)†† ( ion tÈtrathionate incolore† /† ion thiosulfate incolore)
S4O62-(aq)† +† 2 e-† =† S2O32-(aq)
†††††††† * couple :† O2 (g) /† H2O(l)††††††††† O2 (g)† +† 4 e-† +† 4 H+(aq)† =†† 2† H2O(l)
†††††††† * couple :† Cr2O72-(aq)† /† Cr3+(aq)†† : ††† (ion dichromate orange / ion chrome III vert ) :
Cr2O72-(aq)† est un oxydant en milieu acide†
†Cr2O72-(aq)† + 14 H+(aq) + 6 e-† =† 2† Cr3+(aq) + 7 H2O(l)†††††††† (alcootest)
†††††††† * couple : NO3-(aq) / NO(g)††† ( ion nitrate incolore† / gaz monoxyde d'azote)
NO3-(aq) + 3 e- + 4 H+(aq)† =† NO(g) + 2 H2O(l)
†††††††† * couple : IO3-(aq) / I-(aq)††† ( ion iodateÖÖÖÖ/ ion iodure incolore) en milieu basique
On Ècrit d'abord l'Èquation en milieu acide :
IO3-(aq) + 6 e- + 6 H+(aq)† =† I-(aq)† + 3 H2O(l)
On ajoute ensuite des 2 cÙtÈs autant d'ions HO-† que d'ions H+ dÈj‡ prÈsents.
H+(aq) + HO-(aq) = H2O(l) . On remplace directement dans l'Èquation.
Ici , on ajoute 6 HO-†
IO3-(aq) + 6 e- + 6 H2O(l)†† =† I-(aq)† + 3 H2O(l) + 6 HO-(aq)
IO3-(aq) + 6 e- + 3 H2O(l)†† =† I-(aq)† 6 HO-(aq)
©Sciences Mont Blanc