Sujet Bac Antilles Juin 2005
Calculatrice NON autorisée
I ) Jeu de fête foraine (5,5 points)
II ) Détermination d'une constante d'équilibre par deux méthodes (6,5 points)
III ) Sonde thermique (4 points)
III ) Modulation d'amplitude (spe) (4 points)
Antilles Juin 2005 - I ) Jeu de fête foraine :
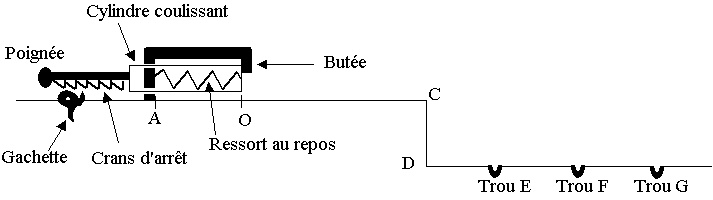
Le but du jeu est d'envoyer une bille d'acier dans un trou. Pour lancer la
bille, le joueur comprime un ressort, ŕ spires non jointives, qui va le propulser
lors de la détente. La bille roule ensuite sur un plan horizontal suivant
la droite (AC), quitte ce plan pour chuter dans un des trous du sol. Le schéma
du dispositif est représenté ci-dessous : (schéma non ŕ l'échelle).
Etudions le mouvement de la bille, objet ponctuel, dans un référentiel terrestre supposé galiléen.
On néglige les frottements.
Données :
- intensité de la pesanteur : g = 10 m.s-2
- masse de la bille m = 10 g
- constante de raideur du ressort : k = 25 N.m-1
- masse du ressort : négligeable devant la masse de la bille.
Aide mathématique : ![]() 10n = 10n / 2
10n = 10n / 2
I ) Propulsion de la bille :
Initialement, le ressort est au repos. Le joueur tire la poignée (compression du ressort) et la bloque avec la gâchette.
Il place la bille contre le cylindre en A', abscisse xA' = - 10 cm sur l'axe (Ox).

1) Exprimer et calculer l'énergie potentielle élastique Epe(A') acquise par le ressort une fois comprimé. (Donner la valeur de Epe(A') avec deux chiffres significatifs)
Le joueur appuie sur la gâchette, le ressort se détend et reprend sa position initiale ; le cylindre arręte son mouvement sur la butée. La bille reste en contact avec le cylindre durant la détente jusqu'au point O. La bille se déplaçant sur un plan horizontal, son énergie potentielle de pesanteur est constante et on la prendra égale ŕ zéro.
2) Quelle forme d'énergie acquiert la bille lors de la détente du ressort ?
Donner son expression littérale en précisant les unités.
3) Donner l'expression littérale de l'énergie mécanique du systčme {ressort-bille}.
4) Que peut-on dire de l'énergie mécanique sachant que les frottements sont négligeables ?
5) Quelle est la valeur de l'énergie cinétique de la bille au point O ? Justifier la réponse.
6) Déduire l'expression littérale de la vitesse v. Calculer la valeur de la vitesse de la bille vO au point O.
La bille se déplace ensuite jusqu'au point C suivant la droite (OC).
7) La vitesse de la bille en C est-elle égale ŕ la vitesse vO ? Justifier la réponse.
II ) Chute de la bille :
La bille quitte ŕ la date t = 0 le plan en C avec une vitesse vC égale ŕ 5,0 m.s-1 et de direction horizontale.

1) Etablir l'expression vectorielle de l'accélération de la bille ŕ partir du bilan des forces.
2) Donner les composantes du vecteur accélération dans le repčre orthonormé (D, x, y).
3) Etablir les équations-horaires x(t) et y(t) du mouvement.
4) Déterminer les expressions littérale et numérique de l'équation y(x) de la trajectoire de la bille.
5) En déduire l'abscisse du trou dans lequel tombe la bille.
©Sciences Mont Blanc
Antilles Juin 2005 -II ) Détermination
d'une constante d'équilibre par deux méthodes :
Quelques valeurs numériques pouvant aider ŕ la résolution des calculs:
|
log(2,0.10-4) = - 3,7 |
2 / 2,3 = 0,87 |
2 / 2,7 = 0,74 |
2 / 3 = 0,67 |
(10a)b = 10a.b |
|
1,0.10-3 = 10.10-4 |
(1,25)2 = 1,56 » 1,6 |
4 / 2,5 = 1,6 |
5 / 4 = 1,25 |
100 / 1,25 = 80 |
I ) La transformation chimique étudiée :
L'acide éthanoďque CH3CO2H , également appelé acide acétique, réagit de façon limitée avec l'eau selon l'équation chimique :
CH3CO2H(aq) + H2O(l) = CH3CO2-(aq) + H3O+(aq)
1) Donner la définition d'un acide selon Brönsted.
2) Dans l'équation ci-dessus, identifier puis écrire les deux couples acide/base mis en jeu.
3) Exprimer la constante d'équilibre K associée ŕ l'équation de cet équilibre chimique.
II ) Etude pH-métrique :
Une solution d'acide éthanoďque, de concentration molaire initiale c1 = 2,7.10-3 mol.L-1 et de volume V1 = 100 mL
a un pH de 3,70 ŕ 25°C.
1) Déterminer la quantité de matičre initiale d'acide éthanoďque n1.
2) Compléter le tableau d'avancement (ŕ rendre avec la copie) en fonction de n1 , xmax ou xf . Exprimer puis calculer l'avancement maximal théorique noté xmax . Justifier la réponse.
|
Equation chimique |
CH3CO2H(aq) + H2O(l) = CH3CO2-(aq) + H3O+(aq) |
||||
|
Etat du systčme |
Avancement (mol) |
Quantités de matičre (mol) |
|||
|
Etat initiale |
|||||
|
En cours de transformation |
|||||
|
Etat final si transformation limitée |
|||||
|
Etat final si transformation totale |
|||||
3) Déduire, de la mesure du pH, la concentration molaire finale en ions oxonium de la solution d'acide éthanoďque.Exprimer puis calculer l'avancement final expérimental de la réaction noté xf
4) Donner l'expression littérale du taux d'avancement final t1 de la réaction. Vérifier, en posant l'opération, que t1 est égal ŕ 7,4.10-2
La transformation étudiée est-elle totale ? Justifier la réponse.
5) a) Exprimer puis calculer la concentration molaire finale en ions éthanoate CH3CO2-(aq) .
b) Exprimer la concentration molaire finale effective de l'acide éthanoďque [CH3CO2H]f .
Calculer sa valeur.
6) Vérifier, en posant l'opération, que la valeur de la constante d'équilibre K1 associée ŕ l'équation de cet équilibre chimique est égale ŕ 1,6.10-5 .
III ) Etude conductimétrique :
On mesure ensuite, ŕ 25°C, la conductivité d'une solution d'acide éthanoďque de concentration c2 = 1,0.10-1 mol.L-1 . Le conductimčtre indique s = 5,00.10-2 S.m-1 .
On rappelle l'équation de la réaction entre l'acide éthanoďque et l'eau :
CH3CO2H(aq) + H2O(l) = CH3CO2-(aq) + H3O+(aq)
1) On néglige toute autre réaction chimique. Citer les espčces ioniques majoritaires présentes dans cette solution. Donner la relation liant leur concentration molaire.
2) Donner l'expression littérale de la conductivité s de la solution en fonction des concentrations molaires finales en ions oxonium et en ions éthanoate.
3) Donner l'expression littérale permettant d'obtenir les concentrations molaires finales ioniques en fonction de s, l(H3O+) , l(CH3CO2-).
Déterminer la valeur de la concentration molaire finale en ions oxonium et éthanoate en mol.m-3, puis en mol.L-1 .
Données : l(H3O+) = 35,9.10-3 S.m2.mol-1 ; l(CH3CO2-) = 4,1.10-3 S.m2.mol-1
4) L'expérimentateur affirme que dans le cas présent, la solution d'acide éthanoďque est suffisamment concentrée pour pouvoir faire les approximations suivantes :
Approximation 1 : la concentration molaire finale en ions éthanoate est négligeable devant la concentration initiale en acide éthanoďque. Ceci se traduit par l'inégalité : [CH3CO2-]f < c2 / 50
Approximation 2 : la concentration molaire finale en acide éthanoďque est quasiment égale ŕ la concentration initiale en acide éthanoďque : [CH3CO2H]f » c2 .
a) Comparer les valeurs de c2 et [CH3CO2-]f (calculée ŕ la question III) 3)).
L'approximation n°1 est-elle justifiée ?
b) En supposant que l'approximation n°2 soit vérifiée, que peut-on dire de la dissociation de l'acide ? En déduire si la transformation chimique est totale, limitée ou trčs limitée. Justifier la réponse.
c) En tenant compte de l'approximation n°2, vérifier, en posant l'opération, que la valeur de la constante d'équilibre K2 associée ŕ l'équation de cet équilibre est égale ŕ 1,56.10-5 .
d) Le taux d'avancement final pour la solution considérée est donné par l'expression : t2 = [CH3CO2-]f / c2
Vérifier en posant l'opération, que le taux d'avancement final de la réaction t2 est égal ŕ 1,25.10-2
IV ) Conclusion : Comparaison des résultats obtenus :
On vient d'étudier deux solutions d'acide éthanoďque de concentrations initiales différentes.
Les résultats sont rassemblés dans le tableau ci-dessous :
|
Concentration molaire initiale d'acide éthanoďque |
Constante d'équilibre |
Taux d'avancement final |
|
|
Etude pH-métrique |
c1 = 2,7.10-3 mol.L-1 |
K1 = 1,6.10-5 |
t1 = 7,40.10-2 |
|
Etude conductimétrique |
c2 = 1,0.10-1 mol.L-1 |
K1 = 1,6.10-5 |
t2 = 1,25.10-2 |
1) La constante d'équilibre K dépend-elle de la concentration initiale en acide éthanoďque ?
Justifier la réponse ŕ partir du tableau.
2) Le taux d'avancement final de la transformation chimique limitée dépend-il de l'état initial du systčme chimique ? Justifier la réponse ŕ partir du tableau.
3) Un élčve propose les deux affirmations suivantes. Préciser si elles sont justes ou fausses, une justification est attendue.
Affirmation 1 : Plus l'acide est dissocié et plus le taux d'avancement final t est grand.
Affirmation 2: Plus la solution d'acide éthanoďque est diluée, moins l'acide est dissocié.
©Sciences Mont Blanc
Antilles Juin 2005 - III ) Sonde thermique :
On peut constituer une sonde thermique ŕ l'aide d'un dipôle (R,C) série. On réalise le circuit suivant :
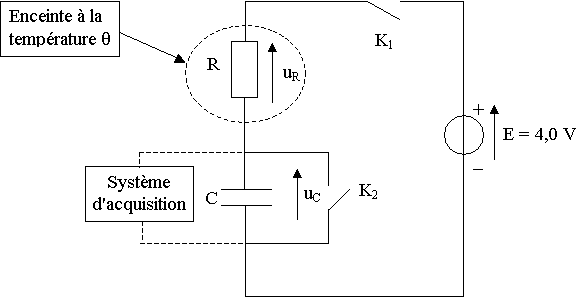
Le condensateur a une capacité C = 1,0 mF.
Le conducteur ohmique est une thermistance : la valeur R dépend de la température. On le place dans une enceinte dont la température interne est notée q.
Un systčme d'acquisition permet d'enregistrer l'évolution au cours du temps de la tension uC aux bornes du condensateur.
Aide mathématique :
|
0,63 x 4,0 = 2,5 |
0,37 x 4,0 = 1,5 |
e0 = 1 |
lim ex = 0 x ® - Ą |
I ) Etalonnage de la soude :
Protocole expérimental :
On souhaite tracer la courbe de l'évolution de la valeur de la résistance de la thermistance en fonction de la température. On réalise le protocole suivant :
Le condensateur est initialement déchargé et les deux interrupteurs K1 et K2 sont ouverts.
A t = 0, on ferme K1 et on enregistre l'évolution de la tension uC jusqu'ŕ la fin de la charge du condensateur. Ensuite, on ouvre K1 et on ferme K2 : le condensateur se décharge complčtement. On ouvre enfin K2.
On modifie la température de l'enceinte et on recommence le protocole précédent. On opčre pour plusieurs valeurs de température et on obtient le graphique suivant :

A l'aide des résultats expérimentaux, étudions la charge du condensateur.
1) Etablir la relation entre la tension E aux bornes du générateur, la tension uR aux bornes du conducteur ohmique et la tension uC aux bornes du condensateur.
2) Déterminer l'équation différentielle vérifiée par la tension uC pendant la phase de charge.
3) La solution analytique de cette équation est de la forme : uC = A + B.e –t / (R.C)
a) En tenant compte des conditions finales de la charge, déterminer A.
b) En tenant compte des conditions initiales de la charge, déterminer B.
c) Déduire l'expression de uC.
4) On donne l'expression de la constante de temps du dipôle (R,C) : t = R.C
a) Vérifier par analyse dimensionnelle l'homogénéité de cette formule.
b) Déterminer la valeur t1 de la constante de temps, relative ŕ la température q1 = 20°C, ŕ partir du graphique. Expliquer la méthode employée.
c) En déduire la valeur R1 de la résistance correspondante.
d) Procéder de la męme maničre pour les autres températures et compléter le tableau ŕ rendre avec la copie. ( Seules les cases blanches sont ŕ compléter)
|
Température q(°C) |
q1 = 20 |
25 |
30 |
35 |
40 |
45 |
50 |
55 |
60 |
|
Constante de temps t (ms) |
t1 = |
||||||||
|
Résistance R (k W) |
R1 = |
1,07 |
0,74 |
0,49 |
0,34 |
e) Tracer sur papier millimétré ( ŕ rendre avec la copie) la courbe d'étalonnage R = f(q) en respectant l'échelle suivante : abscisse : 1 cm pour 5°C ; ordonnée : 1 cm pour 0,1 kW
II ) Mesure d'une température :
Essayons la sonde thermique en la plaçant dans une enceinte de température interne q ŕ déterminer. On mesure la résistance de la thermistance ŕ l'aide d'un ohmmčtre et on obtient :
R = 0,50 kW. En vous servant de la courbe d'étalonnage, déterminer la température de l'enceinte.
©Sciences Mont Blanc
Antilles Juin 2005 - III ) Modulation d'amplitude
(spe) :
Quelques valeurs numériques pouvant ętre nécessaire ŕ la résolution des calculs :
|
6,75 / 40 = 0,169 |
4,5 / 13 = 0,346 |
40 / 6,75 = 5,93 |
|
1 / 4,5 = 0,222 |
1 / 0,346 = 2,89 |
1 / 2,25 = 0,444 |
Les ondes électromagnétiques ne peuvent se propager dans l'air sur de grandes
distances que dans un domaine de fréquences élevées. Les signaux sonores audibles
de faibles fréquences sont convertis en signaux électriques de męme fréquence
puis associés ŕ une onde porteuse de haute fréquence afin d'assurer une bonne
transmission.
I ) La chaîne de transmission :
Le schéma 1 suivant représente la chaîne simplifiée de transmission d'un son par modulation d'amplitude. Elle est constituée de plusieurs dispositifs électroniques.

1) Parmi les cinq propositions ci-dessous, retrouver le nom des quatre dispositifs électroniques numérotés.
Dispositifs électroniques : Antenne, amplificateur HF (Haute fréquence), générateur HF (haute fréquence), multiplieur, voltmčtre.
2) Quels sont les signaux obtenus en B, C et D parmi ceux cités ci-dessous ?
- Porteuse notée uP(t) = UP (max).cos(2p.F.t)
- Signal modulant BF noté uS(t) + U0
- Signal modulé noté um(t)
3) Le signal électrique recueilli en A ŕ la sortie du microphone correspond ŕ la tension électrique uS(t). Une boîte noire est intercalée entre les points A et B. Quel est son rôle ?
4) Le dispositif électrique (2) effectue une opération mathématique simple qui peut ętre :
- (uS(t) + U0) + uP(t)
- (uS(t) + U0) x uP(t)
Choisir la bonne réponse sachant que l'expression mathématique du signal obtenu est :
um(t) = k.(U0 + uS(t)).UP (max).cos(2p.F.t)
II ) La modulation d'amplitude :
La voie X d'un oscilloscope bicourbe est reliée en B et la voie Y est reliée en D. L'oscillogramme obtenu est le suivant :

1) Estimer les valeurs des périodes TS et TP du signal modulant et de la porteuse.
2) Rappeler l'expression théorique de la fréquence f en fonction de la période T avec les unités, puis calculer les fréquences f du signal modulant et F de la porteuse.
3) L'amplitude de la tension du signal modulé um(t) varie entre deux valeurs extręmes, notées respectivement Um (max) et Um (min) Le taux de modulation m s'exprime par :
m = (Um (max) – Um (min)) / (Um (max) + Um (min))
a) Calculer les valeurs des tensions maximale Um (max) et minimale Um (min) du signal modulé.
b) En déduire la valeur de m.
c) A quoi correspondrait un taux de modulation m supérieure ŕ 1 ?
4) Le taux de modulation s'exprime aussi en fonction de la tension maximale du signal modulant US (max) et de la tension U0 selon l'expression suivante : m = US (max) / U0
a) Quelle condition doit-on satisfaire pour obtenir un taux de modulation m < 1 ?
b) Quelle autre condition est nécessaire pour obtenir une bonne modulation ?
c) L'analyse en fréquence du signal montre que celui-ci est composé de trois fréquences f1, f2, f3.
En fonction de la fréquence du signal modulant f et de la fréquence de la porteuse F, exprimer les fréquences apparaissant sur le spectre ci-dessous.

©Sciences Mont Blanc