Sujet Baccalauréat France - Juin 2007
Calculatrice interdite ![]()
II ) Découvertes liées à des éclipses de Soleil ( 6,5 points)
III ) Synthèse d'un ester ( 4 points)
I ) Synthèse d'un conservateur (4 points) (spe)
Sujet Bac France - Juin 2007 - I ) La galiote :
La galiote était un navire de guerre qui fit son apparition ŕ la fin du XVIIčme sičcle, sous le rčgne de Louis XIV. Les galiotes possédaient de lourds canons, fixés au pont, projetant des boulets de 200 livres (environ 100 kg) portant jusqu’ŕ 1200 toises (environ 2400 m).
Selon la description détaillée de Renau, Inspecteur Général de la Marine, ces bâtiments sont destinés ŕ emporter des canons en mer. Ils sont de moyenne grandeur et ŕ fond plat. De par leur fabrication, l’angle de tir des canons est fixe et a pour valeur α = 45°, ce qui permet de tirer ŕ la plus grande distance possible.
La structure d’une galiote doit ętre trčs robuste pour résister ŕ la réaction considérable du boulet et leur échantillon(1) est ordinairement aussi fort que celui d’un vaisseau de 50 canons.
(1) dimension et épaisseur des pičces utilisées pour la construction.
D’aprčs le site Internet de l’Institut de Stratégie Comparée.
Les parties 1, 2 et 3 de cet exercice sont indépendantes.
Certaines aides au calcul peuvent comporter des résultats ne correspondant pas au calcul ŕ effectuer.
1) Action de la poudre de canon sur le boulet
L’éjection du boulet est provoquée par la combustion de la poudre. Une force de poussée est donc exercée sur le boulet par l’ensemble {galiote + canon + gaz}.
Justifier l’expression soulignée dans le texte encadré ci-dessus, ŕ l’aide d’une des trois lois de Newton. Énoncer cette loi. (On pourra s’aider d’un schéma).
2) La trajectoire du boulet
On souhaite étudier la trajectoire du centre d’inertie G du boulet de masse m. L’étude est faite dans le référentiel terrestre considéré comme galiléen.
Le repčre d’étude est (O,  ,
,  )
et l’origine des dates est choisie ŕ l’instant oů le boulet part du point
O (voir figure 1 ci-dessous).
)
et l’origine des dates est choisie ŕ l’instant oů le boulet part du point
O (voir figure 1 ci-dessous).
Le vecteur vitesse initiale![]() G
du point G est incliné d’un angle α
(appelé angle de tir) par rapport ŕ l’horizontale.
G
du point G est incliné d’un angle α
(appelé angle de tir) par rapport ŕ l’horizontale.
Une fois le boulet lancé, la force de poussée de la partie précédente n’intervient plus.

Données :
Volume du boulet : V = 16 dm 3 = 16 L
Masse du boulet : m = 100 kg
Valeur du champ de pesanteur : g = 10 m.s – 2
Masse volumique de l’air : ρ = 1,3 kg.m – 3
|
Aide au calcul |
|||
|
1,6 x 1,3 = 2,1 |
|
||
|
1,6 / 1,3 = 1,2 |
1,3 / 1,6 = 0,81 |
|
|
2.1) Inventaire des forces agissant sur le boulet aprčs son lancement
2.1.1) La poussée d’Archimčde
Donner l’expression littérale de la valeur FA de la poussée d’Archimčde puis la calculer.
2.1.2) Le poids
Calculer la valeur P du poids du boulet aprčs avoir précisé son expression littérale.
2.1.3) Dans cet exercice, on pourra négliger la poussée d’Archimčde devant le poids si la valeur de ce dernier est au moins cent fois plus grande que celle de la poussée d’Archimčde. Montrer que l’on est dans cette situation.
2.1.4) Pendant le vol, compte tenu de la masse, de la vitesse et de la forme du boulet, on fait l’hypothčse que les forces de frottement dans l’air sont négligeables devant le poids. En tenant compte de la remarque et des résultats précédents, établir le bilan des forces exercées sur le systčme {boulet} pendant le vol.
2.2) Equation de la trajectoire
Dans toute cette partie, on négligera la poussée d’Archimčde et on ne tiendra pas compte des forces de frottement dues ŕ l’air.
2.2.1) En appliquant la deuxičme loi de Newton, montrer que les équations horaires du mouvement du point G s’écrivent :
x(t) = (v0 .cos α) . t et y(t) = - ˝ g . t2 + (v0 . sin α) . t
2.2.2) Montrer que l’équation de la trajectoire peut se mettre sous la forme y(x) = Ax2 + Bx.
On donnera les expressions littérales de A et B et on précisera leurs unités respectives.
2.3) Portée du tir
L’équation de la trajectoire du boulet peut se mettre sous la forme y(x) = x × (Ax + B).
Au cours d’un tir d’entraînement, un boulet tombe dans l’eau.
Dans ces conditions, la distance entre le point de départ du boulet et son point M d’impact sur l’eau est appelée portée (voir figure 1 page 2).
On négligera la différence d’altitude entre les points O et M devant les autres distances.
2.3.1) Exprimer la portée d du tir en fonction de A et B.
2.3.2) L’expression littérale de la portée d en fonction de v0 , α et g est : d = v02 . sin 2 α / g
Retrouver, en la justifiant, la valeur α = 45° donnée dans le texte, pour laquelle la portée est maximale, pour une vitesse v0 donnée.
2.3.3) A partir de la question précédente et des données, calculer la vitesse initiale du boulet pour atteindre la portée maximale donnée dans le texte.
2.3.4) En fait, les frottements dans l’air ne sont pas négligeables.
Avec un angle de tir restant égal ŕ 45°, la vitesse initiale du boulet doit-elle ętre supérieure ou inférieure ŕ celle trouvée ŕ la question 2.3.3. pour obtenir la męme portée maximale ? Justifier sans calcul.
3) Restauration d’un boulet par électrolyse
Un boulet est retrouvé par un archéologue, qui le restaure par électrolyse en solution basique.
Ce procédé a pour but, notamment :
- d’éliminer la gangue (substance qui forme une enveloppe autour d'une autre matičre) qui entoure le boulet ;
- de débarrasser l’objet de tous les ions chlorure qui, au contact de l’humidité de l’air et du dioxygčne amčnent ŕ la formation d’acide chlorhydrique conduisant ŕ la destruction rapide du boulet. Ces ions chlorure sont également présents dans la gangue.
Le schéma de principe de l’électrolyse est le suivant :

La lente destruction de la gangue libčre dans l’électrolyte les ions chlorure qu’elle contenait.
L’équation de la réaction modélisant l’électrolyse est :
2 Cl- (aq) + 2 H2O (l) = Cl2 (g) + H2 (g) + 2 HO- (aq)
Les couples d’oxydoréduction mis en jeu sont : Cl2 (g) / Cl- (aq) et H2O (l) / H2 (g)
3.1) La réaction se produisant ŕ l’anode est-elle une oxydation ou une réduction ?
3.2) Ecrire l’équation de la réaction ayant lieu ŕ l’anode.
A quelle borne du générateur est reliée cette électrode ?
3.3) A l’une des électrodes, on observe un dégagement de dihydrogčne.
L’équation de la réaction électrochimique associée est :
2 H2O (l) + 2 e- = H2 (g) + 2 HO- (aq) (1)
La pression exercée par le dihydrogčne permet de décoller la gangue. L’élimination de la gangue se fait sous une intensité I constante et pendant une durée Δt qui dépendent, entre autres, de la nature de l’objet et de son état de corrosion.
Données :
Charge élémentaire : e = 1,6 x 10 –19 C Constante d’Avogadro : NA = 6,0 x 10 23 mol – 1
Intensité du courant : I = 1,0 A Durée de l’électrolyse : Δt = 530 heures
|
Aide au calcul |
|||
|
5,3 x 3,6 ≈ 19 |
2 x 1,6 x 6 ≈ 19 |
5,3 / 3,6 = 1,5 |
2 x 6 / 1,6 = 7,5 |
On note Q la valeur absolue de la charge électrique totale ayant circulé dans le dispositif pendant la durée Δt de l’électrolyse.
3.3.1) Donner l’expression littérale du nombre N d’électrons transférés et celle de la quantité d’électrons n(e–) en fonction des grandeurs données.
3.3.2) Pour simplifier, on fait l’hypothčse que la réaction correspondant ŕ l’équation (1) est la seule ŕ se produire au niveau de l’électrode concernée.
En s’aidant éventuellement d’un tableau d’avancement, établir une relation entre la quantité n(H2) de dihydrogčne dégagé et la quantité d’électrons n(e–) et en déduire que n(H2) = ˝ I . Δt / (e . NA)
3.3.3) Calculer la valeur de n(H2).
3.3.4) En déduire quel serait le volume de dihydrogčne dégagé dans les conditions de l’expérience.
On donne le volume molaire des gaz dans les conditions de l’expérience : VM = 24 L. mol – 1 .
©Sciences Mont Blanc
Sujet Bac France - Juin 2007 - II ) Découvertes liées à des éclipses de Soleil:
Cet exercice se compose de deux parties indépendantes.
Certaines aides au calcul peuvent comporter des résultats ne correspondant pas au calcul ŕ effectuer.
A) Partition lunaire
Des chercheurs du CEA de l’équipe d’Elisabeth Blanc viennent d’annoncer qu’une éclipse n’a pas pour seul effet une baisse de la luminosité. Lors de l’éclipse du Soleil du 11 aoűt 1999, ŕ 12 h 16 précises, l’ombre de la Lune commence sa traversée de la France ŕ la vitesse de 2850 km.h –1 sur un axe Cherbourg-Strasbourg.
Sur son passage, la température de l’air chute rapidement d’environ 5 °C. Le déplacement de cette zone froide, ŕ la męme vitesse que celui de l’ombre (…), engendre dans son sillage des ondes transversales dont la fréquence est largement inférieure ŕ 20 Hz.
D’aprčs la revue Les Défis du CEA - n° 97 octobre-novembre 2003
1) Ondes créées lors de l’éclipse
1.1) Définir une onde mécanique progressive.
1.2) Définir une onde transversale.
1.3) Dire, en justifiant la réponse, si les ondes créées lors de l’éclipse peuvent ętre sonores.
2) Caractéristiques des ondes créées
L’équipe en charge du projet a pu détecter ŕ faible altitude, une série d’ondes dont la période moyenne est de l’ordre de 10 minutes et la célérité moyenne est de l’ordre de 100 km.h – 1.
2.1) Vérifier que la fréquence de l’onde est effectivement largement inférieure ŕ 20 Hz.
2.2) Ces ondes peuvent-elles ętre diffractées par des montagnes séparées par une distance de 10 km ? Justifier la réponse.
|
Aide au calcul |
|
|
1 / 6 = 1,7.10-1 |
1 / 36 = 2,8.10-2 |
B) Découverte historique d’un nouvel élément chimique
Lors de l’éclipse totale du Soleil du 18 aoűt 1868, le français Pierre Janssen et le britannique Norman Lockyer ont analysé le spectre de la couronne solaire et ont remarqué qu’il présentait une raie brillante dans le jaune trčs proche de celle du sodium. N. Lockyer a émis l’hypothčse que cette raie était due ŕ un nouvel élément qu’il baptisa hélium (du grec hélios qui signifie Soleil).
Ce n’est que vingt-sept ans plus tard que cet élément chimique fut identifié sur Terre.
Données :
Célérité de la lumičre dans le vide : c = 2,998 x 108 m.s – 1
Constante de Planck : h = 6,626 x 10 – 34 J.s
1 eV = 1,602 x 10 – 19 J
Longueur d’onde de la raie D du sodium dans le vide : λNa = 589,0 nm.
Longueur d’onde de la raie jaune de l’hélium dans le vide : λHe = 587,6 nm.
|
Aide au calcul |
|
|
6,626 x 2,998 x 1,602 / 589,0 = 5,403 x 10-2 |
6,626 x 2,998 / (587,6 x 1,602 ) = 2,110 x 10-2 |
|
6,626 x 2,998 / (589,0 x 1,602 ) = 2,105 x 10-2 |
6,626 x 2,998 x 1,602 / 587,6 = 5,416 x 10-2 |
1) Spectre d’énergie
1.1) Illustrer, en s’aidant d’un schéma de niveaux d’énergie d’un atome, le phénomčne d’émission d’un photon (quantum d’énergie lumineuse).
1.2) On note E l’énergie du photon émis lors d’une transition énergétique d’un atome.
Donner l’expression littérale de E en fonction de la longueur d’onde λ de la radiation lumineuse émise dans le vide, de la constante de Planck h et de la célérité de la lumičre dans le vide c.
1.3) Raie D du sodium
1.3.1) Calculer la valeur de E en électronvolts, pour le rayonnement correspondant ŕ la raie D du sodium.
1.3.2) Déterminer, en s’aidant de la figure 2 page 7, ŕ quelle transition correspond cette émission.
1.4) L’énergie du photon correspondant ŕ l’émission de la raie jaune de l’hélium (de longueur d’onde λHe) est égale ŕ 2,110 eV.
En s’aidant de la figure 2 page 7, justifier que cette émission ne peut pas ętre attribuée au sodium.
2) Formation de l’hélium dans le Soleil
Les noyaux d’hélium 3 et d’hélium 4 peuvent ętre produits par une suite de réactions nucléaires dont les équations sont indiquées ci-dessous :
11H + 11H → 21H + 01e
11H + 21H → 32He
32He + x2He → 42He + y 11H
2.1) Quel nom donne-t-on ŕ ces réactions nucléaires ?
2.2) Parmi les noyaux 32He , 31H et 42He , lesquels sont isotopes ? Justifier.
2.3) Déterminer les valeurs de x et y dans la troisičme équation de réaction et justifier la réponse en précisant les lois de conservation utilisées.
2.4) On étudie dans la couronne solaire les spectres d’émission des atomes d’hélium 3 et
d’hélium 4. On rappelle qu’un spectre atomique caractérise la configuration électronique de l’atome (c’est-ŕ-dire le nuage d’électrons de l’atome).
2.4.1) Ces deux types d’atomes possčdent-ils la męme configuration électronique ? Justifier.
2.4.2) Ces deux atomes auraient-ils pu ętre distingués l’un de l’autre expérimentalement dans le spectre obtenu par Pierre Janssen et Norman Lockyer ?

©Sciences Mont Blanc
Sujet Bac France - Juin 2007 - III ) Synthèse d'un ester :
L'huile essentielle de Gaulthérie autrement appelée "essence de Wintergreen" est issue d'un arbuste d'Amérique septentrionale : le palommier, également appelé "thé du Canada", "thé rouge", "thé de Terre Neuve". Cette substance est un anti-inflammatoire remarquable. Elle est aussi utilisée en parfumerie et comme arôme dans l’alimentation. Autrefois, elle était obtenue par distillation complčte de la plante.
Cette huile est constituée principalement de salicylate de méthyle. Il est possible de synthétiser cet ester au laboratoire, ŕ partir de l’acide salicylique et du méthanol selon la réaction d’équation :
C7H6O3(s) + CH4O (l) = C8H8O3 (l) + H2O (l)
Cet exercice comporte 13 AFFIRMATIONS concernant un mode opératoire de cette synthčse.
L’aide au calcul peut comporter des résultats ne correspondant pas au calcul ŕ effectuer.
Toute réponse doit ętre accompagnée de justifications ou de commentaires. A chaque affirmation, répondre par VRAI ou FAUX, en justifiant le choix ŕ l’aide de définitions, de schémas, de calculs, d’équations de réactions,…
SI L’AFFIRMATION EST FAUSSE, DONNER LA RÉPONSE JUSTE.
Données :
|
Nom |
Formule |
Masse molaire en g.mol – 1 |
Masse volumique en g.mL– 1 |
Température d’ébullition en °C (pression 1 bar) |
|
Acide salicylique |
C7H6O3 |
M1 = 138 |
&teta;1 = 211 |
|
|
Méthanol |
CH4O |
M2 = 32 |
ρ2 = 0,8 |
&teta;2 = 65 |
|
Salicylate de méthyle |
C8H8O3 |
M3 = 152 |
ρ3 = 1,17 |
&teta;3 = 223 |
|
Cyclohexane |
C6H12 |
M4 = 84 |
ρ4 = 0,78 |
&teta;4 = 81 |
Formule de l’ion hydrogénocarbonate : HCO3-
Masse volumique de l’eau : 1,0 g.mL– 1
Couples acide/base : HCO3-(aq) / CO32- (aq)
CO2 , H2O / HCO3-(aq); le dioxyde de carbone est un gaz peu soluble dans l’eau
|
Aide au calcul |
||
|
1,38 / 2,76 = 0,500 |
2,76 / 1,38 = 2,00 |
2,1 / 7,6 = 0,28 |
|
2,1 / 3,04 = 0,69 |
1,52 / 2,1 = 0,72 |
2,1 / 1,52 = 1,4 |
Dans un ballon, on introduit une masse m1 = 27,6 g d’acide salicylique, un volume V2 d’environ 20 mL de méthanol et 1 mL d’acide sulfurique concentré.
Puis on chauffe ŕ reflux. Sur le flacon de méthanol, on peut
voir les pictogrammes suivants :
|
|
R : 11 - Facilement inflammable. R : 23/25 - Toxique par inhalation et par ingestion. S : 7 - Conserver le récipient bien fermé. S : 16 - Conserver ŕ l'écart de toute flamme ou source d'étincelles - Ne pas fumer. S : 24 - Eviter le contact avec la peau. S : 45 - En cas d'accident ou de malaise consulter immédiatement un médecin. |
|
|
AFFIRMATION 1 : on doit manipuler le méthanol sous la hotte.
AFFIRMATION 2 : le schéma d’un chauffage ŕ reflux est le suivant :
 AFFIRMATION 3 : pour prélever
le méthanol, il faut absolument utiliser une pipette jaugée munie d’une poire
ŕ pipeter (ou propipette).
AFFIRMATION 3 : pour prélever
le méthanol, il faut absolument utiliser une pipette jaugée munie d’une poire
ŕ pipeter (ou propipette).
AFFIRMATION 4 : la quantité n1 d’acide salicylique introduit vaut n1 = 2,00 x 10 – 1 mol.
AFFIRMATION 5 : la quantité n2 de méthanol introduit vaut environ n2 = 5 mol.
AFFIRMATION 6 : l’équation associée ŕ la réaction de synthčse
du salicylate de méthyle s’écrit :
 Acide salicylique |
AFFIRMATION 7 : le réactif introduit en excčs est le méthanol.
Aprčs plusieurs heures de chauffage, on refroidit ŕ température ambiante. On ajoute 100 mL d’eau glacée et on verse dans une ampoule ŕ décanter. On extrait la phase organique avec du cyclohexane. Cette phase a une masse volumique proche de celle du cyclohexane.
AFFIRMATION 8 : la phase organique se situe dans la partie
inférieure de l’ampoule ŕ décanter. ![]()
La phase organique contient l’ester, du méthanol, du cyclohexane et des acides. On lave ensuite plusieurs fois cette phase avec une solution aqueuse d’hydrogénocarbonate de sodium afin d’éliminer les acides restant dans la solution. Il se produit un dégagement gazeux.
AFFIRMATION 9 : le gaz est du dioxyde de carbone.
On effectue ŕ nouveau un lavage ŕ l’eau et on sčche. On sépare les constituants de la phase organique par distillation.
AFFIRMATION 10 : lors de la distillation, le salicylate de méthyle est recueilli en premier.
Aprčs purification, on récupčre une masse m3 = 21 g de salicylate de méthyle.
AFFIRMATION 11 : le rendement de cette synthčse est de 50 %.
AFFIRMATION 12 : l’ajout d’acide sulfurique a permis d’augmenter le rendement de la synthčse.
AFFIRMATION 13 : l’excčs d’un des réactifs a permis d’augmenter le rendement de la synthčse.
©Sciences Mont Blanc
Sujet Bac France - Juin 2007 - I ) Synthèse d'un conservateur (spe)
L’acide benzoďque est un conservateur présent dans de nombreuses boissons sans alcool.
Son code européen est E 210. Il peut ętre préparé par synthčse en laboratoire.
Principe de cette synthčse : l'oxydation, en milieu basique et ŕ chaud de l'alcool benzylique C6H5CH2OH par les ions permanganate MnO4- en excčs, conduit ŕ la formation d'ions benzoate C6H5CO2– et de dioxyde de mangančse MnO2 (solide brun). Cette transformation est totale.
Aprčs réduction, par l'éthanol, des ions permanganate MnO4– excédentaires et élimination du dioxyde de mangančse MnO2, on obtient une solution incolore contenant les ions benzoate.
L'addition d'acide chlorhydrique ŕ cette solution permet la cristallisation de l'acide benzoďque C6H5CO2H (solide blanc), que l'on recueille aprčs filtration, lavage et séchage.
Certaines aides au calcul comportent des résultats ne correspondant pas au calcul ŕ effectuer.
1) Questions relatives au protocole expérimental
1.1) Donner, sans justifier, le nom des parties manquantes (verrerie, nom de montage…), notées de Œ ŕ Ž dans le texte de l’encadré ci-dessous décrivant le protocole expérimental.
1) Formation de l’acide benzoďque :
 Aprčs avoir versé dans un
ballon bicol posé sur un valet et sous la hotte un volume V1
= 2,0 mL d'alcool benzylique puis bouché l’ensemble, on ajoute environ 20
mL de soude de concentration 2 mol.L–1 ŕ l’aide d’ Œ.
On introduit ensuite quelques grains de pierre ponce dans le ballon pour
réguler l’ébullition lors du chauffage.
Aprčs avoir versé dans un
ballon bicol posé sur un valet et sous la hotte un volume V1
= 2,0 mL d'alcool benzylique puis bouché l’ensemble, on ajoute environ 20
mL de soude de concentration 2 mol.L–1 ŕ l’aide d’ Œ.
On introduit ensuite quelques grains de pierre ponce dans le ballon pour
réguler l’ébullition lors du chauffage.
On réalise alors Ť, permettant de chauffer le mélange sans perte de matičre ni surpression.
Aprčs avoir versé lentement une solution aqueuse de permanganate de potassium dans le ballon, on porte le mélange ŕ ébullition douce pendant 10 minutes environ. On ajoute quelques millilitres d'éthanol afin d'éliminer le réactif en excčs, puis on refroidit le ballon et son mélange.
2) Cristallisation de l’acide benzoďque :
On filtre le mélange obtenu, rapidement, en utilisant Ž et on recueille un filtrat limpide et incolore. Le filtrat est ensuite versé dans un becher et refroidi dans la glace.
On ajoute prudemment 8,0 mL d'acide chlorhydrique concentré goutte ŕ goutte et on observe la formation du précipité blanc d'acide benzoďque. On filtre et on rince avec un peu d'eau bien froide.
On récupčre les cristaux d'acide benzoďque sur une coupelle préalablement pesée dont la masse est m = 140,4 g.
On les sčche dans une étuve, puis on pčse l’ensemble et on trouve une masse m’ = 141,8 g.
1.2) Nommer sur la copie les éléments du montage de la figure 3 ci-dessus repérés par les lettres A, B et C.
1.3) Afin de caractériser le produit formé, on réalise une chromatographie sur couche mince.
Dans trois tubes ŕ essais, on verse 1 mL d’éluant E ; dans le tube 1 on ajoute une goutte d’alcool benzylique, dans le tube 2 une pointe de spatule du solide obtenu et dans le tube 3 une pointe de spatule d’acide benzoďque pur.
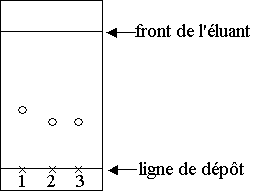 On réalise une chromatographie sur couche
mince ŕ partir du contenu des trois tubes et l’éluant E puis on révčle le
chromatogramme sous rayonnement UV.
On réalise une chromatographie sur couche
mince ŕ partir du contenu des trois tubes et l’éluant E puis on révčle le
chromatogramme sous rayonnement UV.
Interpréter le chromatogramme réalisé lors de la synthčse et conclure quant ŕ la nature du solide obtenu.
2) Rendement de la synthčse
Répondre, dans cette seconde partie, en choisissant la bonne réponse. Justifier clairement ce choix (définition, expression littérale et application numérique, tableau d’avancement …).
Une réponse non justifiée ne sera pas prise en compte.
Données :
|
Nom |
Alcool benzylique |
Permanganate de potassium |
Acide benzoďque |
|
Formule |
C6H5CH2OH |
KMnO4 |
C6H5CO2H |
|
Masse molaire en g.mol – 1 |
M1 = 108 |
M2 = 158 |
M3 = 122 |
|
Masse volumique en g.mL– 1 |
ρ1 = 1,0 |
ρ3 = 1,3 |
2.1) L’oxydation se fait en milieu basique. L’équation chimique de la réaction d’oxydoréduction qui se produit entre l’alcool benzylique et les ions permanganate s’écrit :
3 C6H5CH2OH (l) + 4 MnO4- (aq) = 3 C6H5CO2-(aq) + 4 H2O (l) + 4 MnO2 (s) + HO- (aq)
Les couples oxydant / réducteur mis en jeu lors de la synthčse de l’acide benzoďque sont les suivants : C6H5CO2-(aq) / C6H5CH2OH (l) et MnO4- (aq) / MnO2 (s).
Choisir les deux demi-équations électroniques associées ŕ la transformation décrite ci-dessus.
|
a) C6H5CO2-(aq) + 4 e– + 4 H2O (l) |
= |
C6H5CH2OH (l) + 5 HO- (aq) |
|
b) C6H5CO2-(aq) + 4 e– + 5 H+ (aq) |
= |
C6H5CH2OH (l) + H2O (l) |
|
c) MnO4- (aq) + 8 H+ (aq) + 5 e– |
= |
Mn2+(aq) + 4 H2O (l) |
|
d) MnO4- (aq) + 3 e– + 2 H2O (l) |
= |
MnO2 (s) + 4 HO- (aq) |
|
e) MnO4- (aq) + 3 e– + 4 H+ (aq) |
= |
MnO2 (s) + 2 H2O (l) |
2.2) La quantité n1 d’alcool benzylique contenue dans la prise d’essai de 2,0 mL vaut :
a) n1 = 1,9 x 10 -2 mol ;
b) n1 = 5,4 x 10 - 2 mol ;
c) n1 = 1,9 x 10 - 5 mol.
|
Aide au calcul |
||
|
2,0 / 108 = 1,9 x 10-2 |
108 / 2,0 = 54 |
2,0 x 10-3 = 1,9 x 10-5 |
Pour toute la suite, on précise que la quantité d’ions permanganate apportée vaut n2 = 3,0.10-2 mol.
2.3) Lors de l’oxydation de l’alcool benzylique, les ions permanganate doivent ętre introduits en excčs.
Choisir la bonne proposition (on pourra s’aider d’un tableau d’évolution du systčme).
a) Les ions permanganate ont été introduits en excčs.
b) Les ions permanganate n’ont pas été introduits en excčs.
|
Aide au calcul |
|
|
1,9 / 3 = 0,63 |
1,9 x 3 = 5,7 |
2.4). Lors de la cristallisation, le passage des ions benzoate ŕ l’acide benzoďque se fait selon l’équation chimique :
C6H5CO2-(aq) + H3O+ = C6H5CO2H (s) + H2O (l)
La masse théorique maximale mmax d’acide benzoďque qu’il aurait été possible d’obtenir vaut :
a) mmax = 1,6.10 – 2 g ;
b) mmax = 6,6 g ;
c) mmax = 2,3 g.
|
Aide au calcul |
||
|
1,9 / 122 = 1,6 x 10-2 |
5,4 x 122 = 6,6x 102 |
1,9 x 122 = 2,3 x 102 |
2.5) Le rendement r de la synthčse effectuée vaut :
a) r = 21 % ;
b) r = 61 % ;
c) r = 88 %.
|
Aide au calcul |
||
|
1,4 / 6,6 = 0,21 |
1,4 x 2,3 = 0,61 |
1,4 / 1,6 = 0,88 |
©Sciences Mont Blanc
 2,4 ≈ 1,5
2,4 ≈ 1,5




