Sujet Bac Afrique Juin 2008
Calculatrice autorisée
I ) Autour de la voiture (A - ultrasons) - (B - acide) (7 points)
II ) Pluton et Charon (satellite) (5 points)
III ) La bouteille magique (oxydo-réduction)
(4 points)
III )(spe) De l'eugénol à la vanilline
(4 points)
Sujet Bac Afrique Juin 2008 - I ) Autour de la voiture - Partie A - ultrasons :
Les parties A et B sont indépendantes.
Partie A : Le stationnement « ultra-simple» avec les ultrasons
Les ultrasons sont des ondes mécaniques de période plus courte que les ondes sonores audibles.
Elles ont été découvertes en 1883 par le physiologiste anglais Francis Galton.
Une des nouvelles applications des ultrasons se trouve dans l'industrie automobile, où l'on peut les utiliser afin d'éviter les obstacles.
Certains systèmes permettent de se garer automatiquement en quelques secondes : toute place de stationnement parallèle à la file de circulation disponible et mesurant au moins un mètre quarante de plus que le véhicule est reconnue par les capteurs à ultrasons qui permettent de calculer la trajectoire optimale pour effectuer le créneau sans que le conducteur n'ait à toucher le volant.
1) Généralités sur les ondes sonores
1.1) Donner la définition d’une onde mécanique progressive.
1.2) Les ondes sonores sont un exemple d'ondes mécaniques. Pourquoi une éventuelle communication par onde sonore entre la Terre et la Lune ne serait-elle pas possible ?
1.3) Donner un exemple d'onde pouvant se propager dans le vide.
1.4) Dans le cas d'une onde sonore, la direction de la perturbation est parallèle à celle de la direction de la propagation. Comment peut-on alors qualifier ces ondes ?
2) Détermination de la célérité des ultrasons : 1ère méthode
On alimente un émetteur d'ultrasons en mode « Salve ».
On place face à l'émetteur deux récepteurs A et B comme indiqué sur le schéma simplifié du montage fourni en ANNEXE.
Le récepteur A est relié à la voie EA0 du boîtier d'acquisition, le récepteur B à la voie EA1.
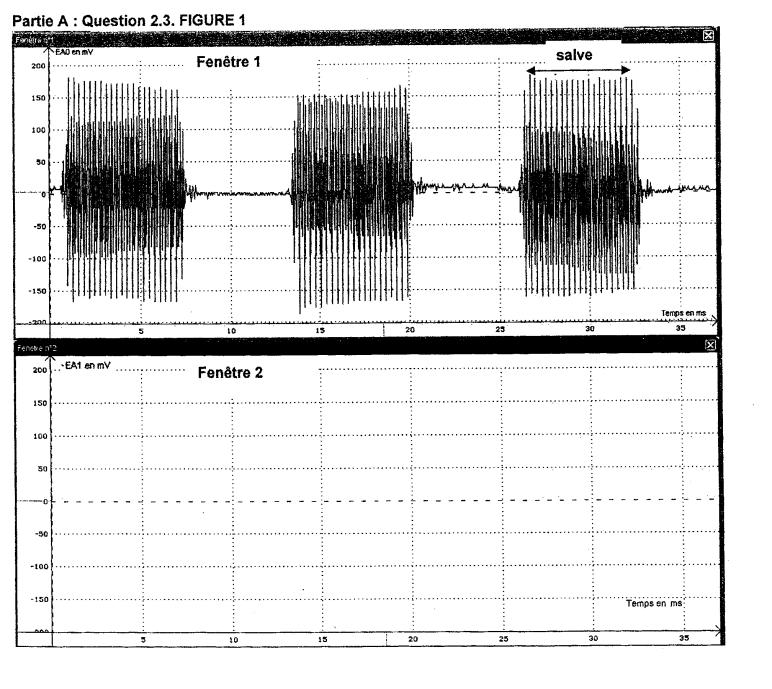
L'enregistrement est présenté en FIGURE 1 DE L'ANNEXE.
La fenêtre 1 correspond au récepteur A, la fenêtre 2 correspond au récepteur B.
2.1) Compléter le schéma simplifié du montage donné en ANNEXE en y faisant apparaître les branchements vers le boîtier d'acquisition.
2.2) Identifier et indiquer dans la fenêtre 1, les zones d'émission sonore et les zones sans émission.
2.3) Positionner les salves de l'acquisition obtenue dans la fenêtre 2 de la FIGURE 1 DE L'ANNEXE. (On ne représentera que leurs enveloppes).
On déplace ensuite le récepteur B, dans la direction émetteur-récepteur, d'une distance d suffisamment grande pour pouvoir mesurer avec précision le retard ultrasonore Δt correspondant au passage de l'onde par les deux récepteurs. Le déplacement s'effectue selon un axe parallèle à l'axe x'x du schéma simplifié du montage.
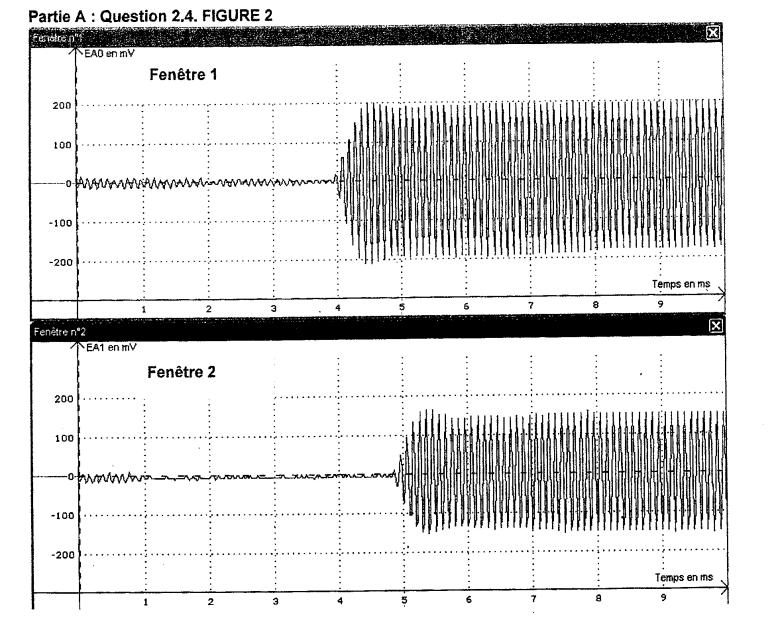
Afin de déterminer la célérité des ondes ultrasonores, on réalise une acquisition (sur une durée inférieure à celle d'une salve) pour une distance d = 0,3 m donnant les enregistrements présentés dans la FIGURE 2 DE L'ANNEXE.
2.4) Indiquer sur la figure 2 le retard Δt correspondant et le mesurer.
2.5) En déduire la valeur V1 de la célérité des ondes ultrasonores dans l'air.
2.6) Obtiendrait-on le même résultat pour la célérité si on effectuait l'expérience en utilisant l'eau à la place de l'air comme milieu de propagation? Justifier.
3) Détermination de la célérité des ultrasons : 2ème méthode
On fait maintenant fonctionner l'émetteur en mode « Continu ».
On visualise cette fois-ci les signaux à l'aide d'un oscilloscope : le récepteur A est relié à la voie 1 et le récepteur B à la voie 2.
Au départ, on place à nouveau les deux récepteurs en face de l'émetteur, côte à côte, comme sur le schéma simplifié du montage de départ.
Les deux signaux sont alors superposés et confondus.
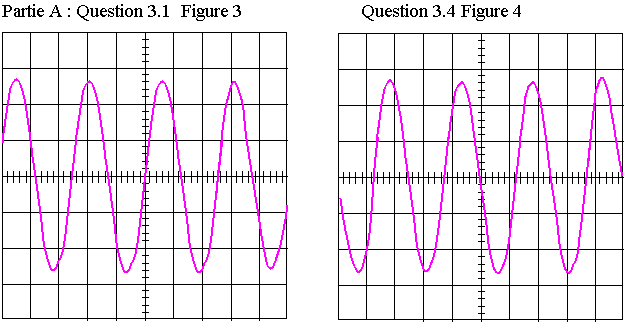
En choisissant une sensibilité verticale de 0,10 V.div-1 et une sensibilité horizontale de 10 µs.div-1 on obtient l'oscillogramme du signal capté par le récepteur A présenté en FIGURE 3 DE L'ANNEXE.
3.1) Déterminer la période et en déduire la fréquence des ultrasons.
3.2) On déplace le récepteur B en l'éloignant du récepteur A, ce dernier étant fixé. Le déplacement s'effectue dans la direction émetteur-récepteur selon un axe parallèle à l’axe x'x du schéma simplifié du montage: les deux sinusoïdes se décalent puis se superposent à nouveau.
On répète l'opération d’éloignement du récepteur B jusqu'à la 10ème superposition des courbes. La distance d1 entre A et B est alors de 8,4 cm.
Utiliser ces données pour déterminer la valeur d'une grandeur caractéristique de l'onde que l'on nommera.
3.3) Utiliser les questions 3.1 et 3.2 pour déterminer une valeur V2 de la célérité des ultrasons.
On précisera la démarche et les calculs effectués.
3.4) On donne sur la FIGURE 4 DE L'ANNEXE. Le signal capté par le récepteur B lorsqu'il a été décalé d'une autre distance d2 par rapport au récepteur A.
On néglige tout amortissement. La distance d2 étant comprise entre 3,5 cm et 4,0 cm, déduire à l'aide de la FIGURE 4 DE L'ANNEXE, la valeur de d2.
4) Détection de distance
Une voiture est équipée d'un système comportant un émetteur et un récepteur d'ultrasons placés côte à côte à l'arrière du véhicule.
Lors d'une marche arrière, une salve ultrasonore est envoyée et réfléchie par un obstacle puis détectée par le récepteur 9,0 ms après l'émission, la célérité du son étant considérée comme égale à 1,2.103 km.h-1.
A quelle distance se trouve l'obstacle de la voiture? Justifier la réponse.
ANNEXE A RENDRE AVEC LA COPIE
Partie A Question 2.1. Schéma simplifié du montage
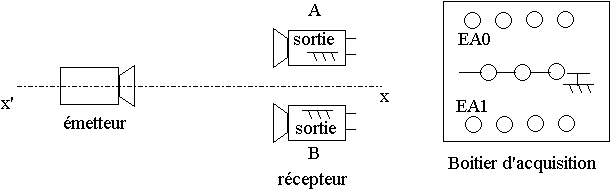
©Sciences Mont Blanc
Sujet Bac Afrique Juin 2008 - I ) Autour de la voiture - Partie B - acide :
Partie B : L'électrolyte utilisé dans la batterie
La batterie d’une voiture est composée de plusieurs cellules d’accumulateurs montées en série. L'électrolyte utilisé est une solution aqueuse d'acide sulfurique concentré. On se propose dans cette partie de mesurer la concentration c en soluté H2SO4 apporté dans cet électrolyte.
1) L'électrolyte S0 étant trop concentré, on se propose de le diluer 1000 fois. On obtient une solution S1.
Choisir, en justifiant parmi le matériel proposé, la verrerie nécessaire pour réaliser cette manipulation :
- fioles jaugées de 10,00 mL, 50,00 ml, 100,00 mL, 1,00 L
- pipettes graduées de 1,0 mL, 2,0 mL, 10,0 ml
- pipettes jaugées de 1,00 mL, 2,00 mL, 10,00 ml
- béchers de 50 mL, 100 mL, 1 L
2) On mesure le pH de la solution S1 : pH = 2,13 ; en déduire la concentration en ions oxonium H3O+(aq) de cette solution
3) En déduire la concentration en ions oxonium de la solution S0.
4) L'électrolyte S0 a été préparé par dissolution de H2SO4 dans l'eau.
La réaction est totale et peut s'écrire :
H2SO4 (l) + 2 H2O(l) = 2 H3O+(aq) + SO42-(aq)
4.1) Compléter le tableau d'avancement donné en ANNEXE.
4.2) Etablir une relation entre la quantité de matière finale nf(H3O+(aq)) d'ions H3O+(aq) et l'avancement maximal xmax de la réaction.
4.3) En déduire une relation entre la quantité de matière initiale ni (H2SO4) de soluté H2SO4 apporté et la quantité finale nf(H3O+(aq)) d'ions H3O+ (aq).
4.4) Montrer que la concentration c en soluté H2SO4 apporté dans l'électrolyte vaut 3,71 mol.L-1.
ANNEXE A RENDRE AVEC LA COPIE
Question 4.1 Tableau d’avancement
|
Equation chimique |
H2SO4 ( l) + 2 H2O ( l) = 2 H3O+(aq) + SO42-(aq) |
||||
|
Etat du système |
Avancement (mol) |
Quantités de matière (mol) |
|||
|
Etat initial |
0 |
ni (H2SO4) |
excès |
0 |
0 |
|
Etat intermédiaire |
x |
excès |
|||
|
Etat final |
xmax |
excès |
|||
©Sciences Mont Blanc
Sujet Bac Afrique Juin 2008 - II ) Pluton et Charon (satellite) :
Pluton a été découverte par l'astronome Clyde W. Tombaugh, le 18 février 1930, après de longs mois d'observations. Pendant 66 ans, elle fut considérée comme la neuvième planète du système solaire. Cependant, depuis une quinzaine d'années, des objets semblables à Pluton de par leur taille et leur masse ont été découverts obligeant l'union astronomique internationale (UAI) à redéfinir la notion de planète.
Depuis le mois d'août 2006, Pluton est classée parmi les planètes naines. Jusqu'en 1978, année de découverte du premier satellite naturel Charon, la masse de Pluton n'était pas connue avec exactitude.
Données :
G = 6,673.10-11 m3.kg-1.s-2
1 année sidérale = 365,2564 jours solaires moyens.
1 jour solaire moyen a une durée égale à 86 400 s.
Les caractéristiques de Pluton et de Charon sont données ci-après:
Tableau n°1 : Caractéristiques de Pluton
|
Rayon à l'équateur (km) |
Distance moyenne au Soleil (km) |
|
1,15. 103 |
5,91.109 |
Tableau n°2 : Caractéristiques de Charon
|
Masse (kg) |
Rayon à l'équateur (km) |
Période de rotation
propre |
Période de révolution autour de Pluton (en jours solaires) |
Distance moyenne au centre de Pluton (km) |
|
1,61.1021 |
6,03.102 |
6,387 |
6,387 |
1,94.104 |
L'objectif de cet exercice est de déterminer la masse de Pluton en utilisant deux hypothèses qui conduiront à deux valeurs de cette masse notées MP1 et MP2.
Les parties 1 et 2 de cet exercice sont indépendantes.
1) Généralités
1.1 ) Définir un mouvement circulaire uniforme.
1.2) Quelles sont les deux conditions nécessaires pour observer un mouvement circulaire uniforme ?
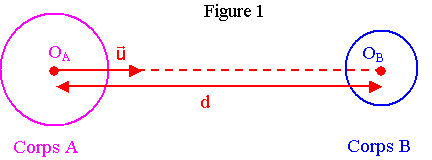
1.3) La figure 1 ci-contre représente deux corps A et B à symétrie sphérique et homogènes en masse, de centres de gravité respectifs OA et OB.
 est un vecteur unitaire.
est un vecteur unitaire.
La distance entre les deux centres de gravité est notée d.
La masse du corps A est notée MA, celle du corps B est notée MB.
Donner l’expression vectorielle de la force d'interaction
gravitationnelle  A → B exercée par le corps A sur le corps
B.
A → B exercée par le corps A sur le corps
B.
2) Etude du système Pluton - Charon
Le référentiel attaché à Pluton est appelé référentiel plutonocentrique.
L'origine du référentiel est le centre de gravité de Pluton et ses axes sont parallèles à ceux du référentiel héliocentrique.
On considère que le référentiel plutonocentrique est galiléen. Les corps célestes Pluton et Charon sont à symétrie sphérique et à répartition uniforme de masse.
On néglige toutes les interactions autres que les interactions entre Pluton et Charon.
On notera MP1 la masse de Pluton, Mc la masse de Charon, P et C les centres de gravité respectifs de Pluton et de Charon.
On fera dans un premier temps l'hypothèse que la masse de Charon est négligeable devant celle de Pluton.
Le centre de gravité de Charon décrit une trajectoire circulaire de rayon R autour de Pluton.
Cette trajectoire est représentée sur la figure 2 ci-dessous. On admet que cette trajectoire est plane.
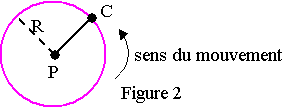 2.1) Période de révolution
2.1) Période de révolution
Pluton met 6,387 jours solaires pour faire un tour sur elle-même et 248 années sidérales pour effectuer un tour autour du Soleil.
Quelle est la période de révolution de Pluton ? Justifier la réponse.
2.2) Etude du mouvement de Charon
2.2.1) En appliquant la seconde loi de Newton au centre d’inertie
de Charon, en déduire les caractéristiques (direction, sens, norme) du vecteur
accélération  du centre d'inertie de
Charon. La norme sera exprimée en fonction des données de l'énoncé.
du centre d'inertie de
Charon. La norme sera exprimée en fonction des données de l'énoncé.
2.2.2) Vérifier que le mouvement circulaire uniforme est une solution de la relation établie à question 2.2.1) et montrer alors que la vitesse du centre d'inertie de Charon est :
v =  (G . MP1 / R )
(G . MP1 / R )
2.2.3) Etablir l'expression de la période de révolution T de Charon autour de Pluton.
2.2.4) Déduire des deux questions précédentes la relation suivante: T2 / R3 = 4 π2 / ( G . MP1 )
2.3) Détermination de la masse de Pluton
2.3.1) A l'aide de la question 2.2.4), expliquer ce qui a permis, à partir de 1978, de déterminer la masse de Pluton.
2.3.2) En utilisant les tableaux de données et la question 2.2.4), calculer la masse MP1 de Pluton.
2.3.3) En réalité, la masse de Charon n'est pas négligeable devant celle de Pluton.
On cherche donc à calculer la masse de Pluton, notée MP2 en tenant compte de cette nouvelle hypothèse.
On montre alors que : T2 / R3 = 4 π2 / ( G . (MP2 + MC )
En déduire la masse MP2 de Pluton.
2.3.4) La valeur admise pour la masse de Pluton est 1,31.1022 kg.
Discuter de la pertinence de l'hypothèse formulée a la question 2.3.3.
©Sciences Mont Blanc
Sujet Bac Afrique Juin 2008 - III ) La bouteille
magique (oxydo-réduction) :
Au cours d’une séance de travaux pratiques, un élève d’une terminale S doit réaliser le mélange réactionnel décrit dans le protocole expérimental suivant.
Protocole expérimental :
Dans un erlenmeyer contenant une solution S dont on ne se souciera pas du contenu, on dissout du glucose.
On ajoute une solution de bleu de méthylène. Cette solution donne une coloration bleue au mélange réactionnel.
On constate que la solution bleue devient progressivement incolore.
Boucher l’erlenmeyer et agiter vigoureusement : la solution devient immédiatement bleue puis se décolore de nouveau lentement.
Agiter une nouvelle fois : la solution devient tout de suite bleue puis se décolore progressivement.
Données du problème :
La seule espèce colorée dans le mélange réactionnel est la forme oxydée du bleu de méthylène qui donne une coloration bleue. Elle est notée BM+(aq).
La forme réduite est notée BMH(aq).
Dans les conditions de l’expérience, le glucose est un réducteur qui réduit le bleu de méthylène. On admettra qu’il est introduit en large excès devant les autres réactifs.
Le glucose est noté RCHO(aq). Sa masse molaire est M = 180 g.mol-1.
Couples oxydant/réducteur :
BM+(aq) / BMH(aq) ; O2 (aq) / H2O(l) ; RCOOH(aq) / RCHO(aq)
1) Equation de la réaction modélisant la transformation chimique entre le glucose et la solution de bleu de méthylène.
1.1) Donner la définition d’un oxydant, puis d’un réducteur.
1.2) Ecrire la demi équation électronique de réduction de la forme oxydée BM+(aq) du bleu de méthylène.
1.3) Ecrire la demi-équation électronique d’oxydation du glucose RCHO(aq).
1.4) En déduire que l’équation d’oxydoréduction entre le glucose et la forme oxydée du bleu de méthylène est :
RCHO(aq) + BM+(aq) + H2O(l) = RCOOH(aq) + BMH(aq) + H+(aq) (équation1)
Cette réaction est lente.
2) Interprétation des observations
Lorsque l’on agite l’erlenmeyer, une partie du dioxygène de l’air se dissout dans la solution puis réagit en oxydant la forme réduite du bleu de méthylène.
L’équation de la réaction modélisant la transformation chimique observée est donnée ci-dessous :
2 BMH(aq) + O2 (aq) + 2 H+(aq) = 2 H2O(l) + 2 BM+(aq) (équation 2)
Cette réaction est rapide et totale.
2.1) A l’aide des caractéristiques des équations chimiques 1 et 2, expliquer les variations de couleur observées lors de l’expérience et leurs vitesses.
2.2) Quels facteurs cinétiques pourrait-on utiliser pour augmenter la vitesse de la réaction décrite dans la partie 1 ?
3) Etude quantitative
L'erlenmeyer dans lequel l'élève réalise l'expérience est bouché hermétiquement et contient un volume V(O2) = 48 mL de dioxygène et 5,0 g de glucose RCHO.
Le volume molaire des gaz dans les conditions de l'expérience vaut Vm = 24,0 L.mol-1.
3.1) Compléter de façon littérale et en respectant les notations, le tableau d'avancement de l'ANNEXE.
3.2) Calculer la quantité de matière initiale ni(O2) de dioxygène contenu dans l'erlenmeyer.
On réalise une série d'agitations successives qui permet de dissoudre tout le dioxygène présent dans l’erlenmeyer.
3.3) En déduire la quantité de matière ni(BMH) susceptible de réagir avec la quantité de matière initiale ni(O2) de dioxygène.
3.4) A partir de l'équation 1, montrer que la quantité de matière de glucose n(RCHO) ayant réagi au cours de l'expérience est 4,0.10-3 mol.
On pourra s'aider d'un tableau d’avancement.
3.5) En déduire la masse m de glucose n'ayant pas réagi dans l'erlenmeyer.
ANNEXE DE L’EXERCICE III
Question 3.1. Tableau d’avancement
|
Equation chimique |
2 BMH(aq) + O2 (aq) + 2H+(aq) = 2 H2O(l) + 2 BM+(aq) |
|||||
|
Etat du système |
Avancement |
Quantités de matière |
||||
|
Etat initial |
0 |
ni (BMH) |
ni (O2) |
excès |
excès |
0 |
|
Etat intermédiaire |
x |
excès |
excès |
|||
|
Etat final |
xmax |
excès |
excès |
|||
©Sciences Mont Blanc
Sujet Bac Afrique Juin 2008 - III ) De l'eugénol
à la vanilline (spe):
Le giroflier est un arbuste cultivé à Madagascar, en Afrique et en Indonésie. Les clous de girofle sont les bourgeons séchés, non éclos, du giroflier et sont parmi les plus anciennes épices et drogues décrites dans l’histoire. L’huile essentielle des clous de girofle contient principalement de l’eugénol, de 75 à 80%, de l’éthanoate d’eugényle, de 4 à 10%, du β-caryophyllène, de 7 à 10% et de faibles quantités d’autres produits. En dehors des usages pharmaceutiques de l’essence de girofle, l’eugénol est utilisé dans l’hémisynthèse industrielle de la vanilline.
La vanille est l’épice la plus utilisée au monde. La vanilline est l’arôme principal des gousses de vanillier. Les gousses contiennent peu de vanilline : 1 kg de gousses de vanille donnent 25 g de vanilline. Compte-tenu du prix de revient élevé de la vanille, la vanilline naturelle est très souvent remplacée par la vanilline de synthèse (dont le prix de revient est environ 300 fois moins élevé). La synthèse de la vanilline se fait en trois étapes dont seulement deux seront présentées dans le problème.
Les parties 1 et 2 sont indépendantes
1) Extraction de l’huile essentielle du clou de girofle
1.1) Pour extraire l’huile essentielle des clous de girofle, dont le principal constituant est l’eugénol, on introduit dans un ballon 100 mL d’eau distillée, 5 g de clous de girofle en poudre et quelques morceaux de pierre-ponce. On met en place le montage d’hydrodistillation, on porte à ébullition et on fait fonctionner jusqu’à recueillir 30 à 40 mL de distillat dans un erlenmeyer.
Parmi les montages de verrerie ci-dessous, identifier celui à utiliser.
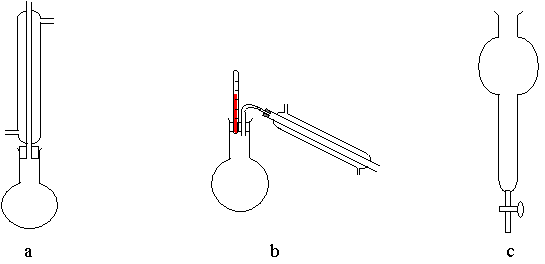
1.2) On transvase le contenu de l’erlenmeyer dans une ampoule à décanter. Sous hotte, on ajoute 10 mL de dichlorométhane.
On agite vigoureusement l’ampoule en dégazant régulièrement.
Pour faciliter l’extraction de l’eugénol, on ajoute environ 50 g de chlorure de sodium au distillat.
On agite jusqu’à dissolution. Après agitation, on enlève le bouchon de l’ampoule et on laisse décanter son contenu.
Données :
Tableau n°1 : Densité et miscibilité à l’eau de quelques solvants organiques
|
A 25°C |
Cyclohexane |
Dichlorométhane |
Éthanol |
|
Densité par rapport à l’eau |
0,89 |
1,34 |
0,78 |
|
Miscibilité à l’eau |
faible |
faible |
très grande |
Tableau n°2: Solubilité de l’eugénol dans différents solvants.
|
Solvant |
Eau |
Eau salée |
Cyclohexane |
Éthanol |
Dichlorométhane |
|
Solubilité |
faible |
Très faible |
grande |
grande |
grande |
1.2.1) Justifier à l’aide des tableaux de données qu’il y a deux phases, l’une que l’on nommera phase organique et l’autre phase aqueuse.
1.2.2) La phase inférieure dans l’ampoule est-elle la phase aqueuse ou la phase organique ? Justifier à l’aide des tableaux de données.
1.2.3) Après agitation, dans quelle phase se trouve l’eugénol ? Justifier à l’aide des tableaux de données.
1.2.4) Pourquoi a-t-on ajouté du chlorure de sodium dans l’ampoule à décanter ?
Justifier à l’aide des tableaux de données.
1.2.5) Les deux autres solvants proposés dans les tableaux sont-ils utilisables pour réaliser l’extraction ? Justifier à l’aide des tableaux de données.
1.3) On réalise une chromatographie sur couche mince de l’huile essentielle extraite des clous de girofle. On dépose sur la plaque, en solution dans le dichlorométhane :
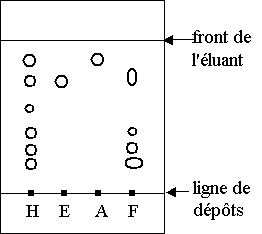
* l’huile essentielle préparée à partir des clous de girofle (H)
* de l’eugénol commercial (E)
* de l’éthanoate d’eugényle (A)
* de l’huile essentielle préparée à partir de feuilles de giroflier (F).
L’éluant est un mélange de toluène et d’éthanol.
1.3.1) L’huile essentielle extraite des feuilles de giroflier contient-elle de l’éthanoate d’eugényle. ? Justifier.
1.3.2) Quelles sont les espèces chimiques pures identifiables contenues dans l’huile essentielle de clous de girofle ?
2) Sur le chemin de la vanilline
2.1) 1ère étape : synthèse de l’éthanoate d’isoeugénol.
Le mode opératoire est le suivant :
* introduire dans un ballon 5,0 g d’isoeugénol, 10 mL d’anhydride éthanoïque et quelques grains de pierre ponce ;
* réaliser le montage pour un chauffage à reflux ; amener le mélange au reflux et le maintenir pendant 40 min ;
* refroidir dans un bain de glace 10 min ;
* verser le contenu du ballon dans 30 mL d’eau glacée et laisser cristalliser l’éthanoate d’isoeugénol ;
*filtrer le solide sur Büchner.
La réaction est représentée par l’équation suivante :
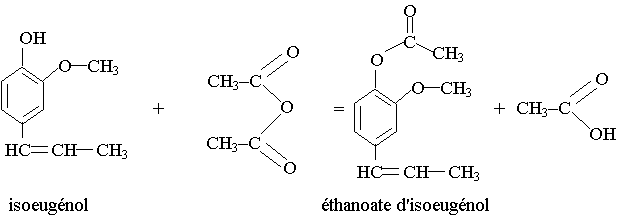
Données :
|
Espèce chimique |
Masse molaire (g.mol-1) |
Quelques propriétés |
|
Isoeugénol |
164 |
d = 1,08 Nocif en cas d’ingestion et irritant pour les yeux, les voies respiratoires et la peau. |
|
Ethanoate d’isoeugénol |
205 |
Tfusion = 80°C Soluble dans la plupart des solvants organiques et insoluble dans l’eau glacée. |
|
Anhydride éthanoïque |
102 |
d =1,08 Corrosif, inflammable, provoque des brûlures. Réagit avec l’eau. |
|
Ethanoate de vanilline |
193 |
Soluble dans le dichlorométhane et insoluble dans l’eau. |
|
Dichlorométhane |
84,9 |
d = 1,34 ; non miscible à l’eau. Ne pas respirer les vapeurs, éviter le contact avec la peau et les yeux. |
2.1.1) Quel est le rôle du chauffage à reflux ?
2.1.2) Pourquoi utilise-t-on un anhydride d’acide plutôt qu’un acide carboxylique pour effectuer cette réaction ?
2.1.3) Pourquoi verse-t-on le contenu du ballon dans de l’eau glacée ?
2.1.4) Calculer la quantité de matière initiale de chacun des réactifs.
2.1.5) Calculer la masse maximale d’éthanoate d’isoeugénol que l’on pourrait obtenir par cette synthèse.
2.1.6) L’expérimentateur a obtenu 5,6 g de cristaux d’éthanoate d’isoeugénol. Le rendement de cette synthèse est défini comme étant le rapport de la masse de produit obtenu expérimentalement sur la masse de produit qui serait obtenu dans l’hypothèse d’une réaction totale. Calculer le rendement de cette synthèse.
2.2) 2ème étape et 3ème étape : synthèse de l’éthanoate de vanilline et obtention de la vanilline
Le mode opératoire relatif à la synthèse de l’éthanoate de vanilline à partir de l’éthanoate d’isoeugénol (2ème étape) ne sera pas explicité.
La dernière étape consiste tout d’abord à dissoudre les cristaux d’éthanoate de vanilline dans un ballon contenant 10 mL d’éthanol et d’ajouter de l’acide chlorhydrique concentré. Après 30 minutes de chauffage à reflux, on refroidit le ballon dans un bain d’eau glacée puis on sépare les phases aqueuse et organique.
La phase organique est séchée, le solvant est évaporé et on récupère un solide sentant la vanille.
La réaction de synthèse de la vanilline
est représentée par l’équation suivante. Il s’agit de l’hydrolyse d’un ester.
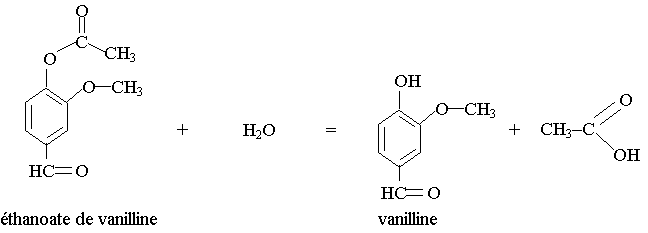
2.2.1) Donner deux caractéristiques de cette réaction.
2.2.2) L’acide chlorhydrique concentré est un catalyseur de la réaction de synthèse de la vanilline.
Qu’appelle-t-on un catalyseur en chimie ?
©Sciences Mont Blanc